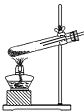
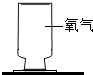
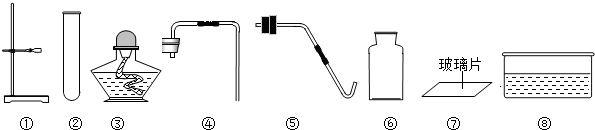
实验室用高锰酸钾制纯净氧气时,下列做法错误的是( )
题目答案
您的答案
答案解析
分析:
A、为了收集的氧气更纯净,应在试管口放一团棉花,防止高锰酸钾粉末进入导管;
B、为防止加热时试管内壁出现的小水珠流到试管底部将试管炸裂,因此试管口要略向下倾斜;
C、导管口的气泡连续、均匀的放出时开始收集,以防收集的氧气不纯;
D、为防止冷水倒吸入热的试管,则在实验完毕后,先将导管移出水面再熄灭酒精灯.
解答:
解:A、为了收集的氧气更纯净,应在试管口放一团棉花,防止高锰酸钾粉末进入导管,故做法正确;
B、为防止加热时试管内壁出现的小水珠流到试管底部将试管炸裂,因此试管口要略向下倾斜,故做法正确;
C、导管口的气泡连续、均匀的放出时开始收集,以防收集的氧气不纯,故做法错误;
D、为防止冷水倒吸入热的试管,则在实验完毕后,先将导管移出水面再熄灭酒精灯,故做法正确.
故选C.
点评:
重在考查加热高锰酸钾制取氧气的操作步骤和各注意事项,难度不大.