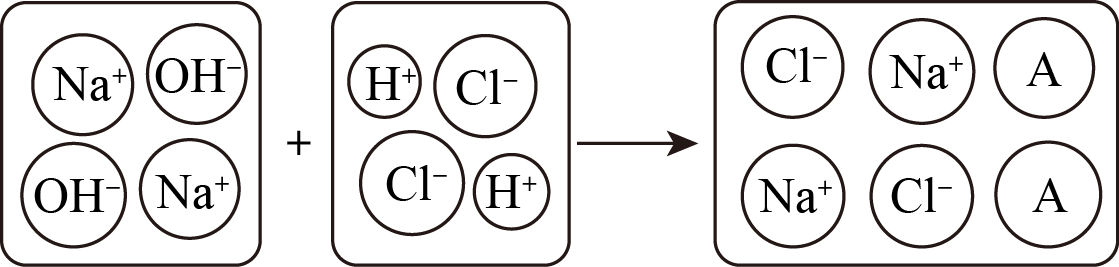
将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如图。由此分析下列说法不正确的是( )
题目答案
您的答案
答案解析
问题要点
$\mathrm{NaOH}+\mathrm{HCl}=\mathrm{NaCl}+\mathrm{H}_{2} \mathrm{O}$
质量守恒定律
答案解析
A.溶液在任何时间都是对外不显电性,所以正确;
B.反应前的溶质时氯化氢和氢氧化钠,反应后的溶质时氯化钠,根据质量守恒定律:$\mathrm{m}_{(\mathrm{NaOH})}+\mathrm{m}_{(H C 1)}=\mathrm{m}_{(\mathrm{NaCl})}+\mathrm{m}_{\left(\mathrm{H}_{2} \mathrm{O}\right)}$,所以反应后的溶质质量减少,所以错误;
C.恰好完全反应之后所得的溶液是氯化钠溶液,氯化钠溶液呈中性,所以正确;
D.反应后的溶液中的微观粒子有:$\mathrm{Na}^{+},\mathrm{Cl}^{-},\mathrm{H}_{2} \mathrm{O}$ ,所以A代表的是水分子,正确;

