苯甲酸是常见的食品防腐剂,某同学准备进行实验,验证苯甲酸具有酸的某一通性,他选择的下列物质中,不能达到实验目的的是( )
题目答案
您的答案
答案解析
酸的通性指的是,酸会与排在氢前面的金属单质、金属氧化物、碱、盐、指示剂发生反应,$\rm A$ 选项金属排在氢之后,故 $\rm A$ 选项无法实现。
故选 $\rm A$。
苯甲酸是常见的食品防腐剂,某同学准备进行实验,验证苯甲酸具有酸的某一通性,他选择的下列物质中,不能达到实验目的的是( )
酸的通性指的是,酸会与排在氢前面的金属单质、金属氧化物、碱、盐、指示剂发生反应,$\rm A$ 选项金属排在氢之后,故 $\rm A$ 选项无法实现。
故选 $\rm A$。
将下列溶液置于敞口容器中,溶液质量会增加的是( )
将足量铁钉放入硫酸铜溶液中,铁钉表面有红色物质析出,且产生少量无色无味的气体。下列说法中正确的是( )
①气体可能是氢气;②气体可能是二氧化硫:③反应后溶液呈浅绿色:④反应后溶液蓝色。
足量铁钉与硫酸铜发生反应方程式为 $\text{Fe}+\text{CuS}{{\text{O}}_4}=\text{Cu}+\text{FeS}{{\text{O}}_4}$。因为 $\text{Fe}$ 过量由溶液可能显酸性,故 $\text{Fe}$ 在酸性环境中放出 ${{\text{H}}_2}$,故①③正确。
A.选①③,故A正确;
B.选①③,故B错误;
C.选①③,故C错误;
D.选①③,故D错误;
故选A。
化学趣味小组在学习了金属的化学性质后,对金属 $\text{R}$ 的活动性进行探究发现:将金属 $\text{R}$ 放入稀盐酸中,观察到有气泡产生(该反应的化学方程式可表示为:$\text{R}+\text{2HCl}=\text{RC}{{\text{l}}_2}+{{\text{H}}_2}\uparrow $),将 $\text{R}$ 放入 $\text{ZnS}{{\text{O}}_2}$ 溶液中无任何变化。下列化学方程式书写错误的是( )
将金属 $\text{R}$ 放入稀盐酸中,观察到有气泡产生,说明 $\text{R}$ 能与稀盐酸反应,即活动性 $\text{R}>\text{H}$;由 $\text{R}+2\text{HC}{{\text{l}}_2}=\text{RC}{{\text{l}}_2}+{{\text{H}}_2}\uparrow $ 可知,$\text{R}$ 在化合物中显 $+2$ 价;
将 $\text{R}$ 放入 $\text{ZnS}{{\text{O}}_4}$ 溶液中无任何变化,说明 $\text{Zn}$ 的金属活动性比 $\text{R}$ 强,即 $\text{Zn}>\text{R}$;
A.由于金属活动性 $\text{Mg}>\text{Zn}>\text{R}$,所以 $\text{R}$ 不能与 $\text{MgS}{{\text{O}}_4}$ 反应,故A错误;
B.由于金属活动性 $\text{R}>\text{H}>\text{Cu}$,所以 $\text{R}$ 能与 $\text{CuS}{{\text{O}}_4}$ 反应,化学方程式 $\text{R}+\text{CuS}{{\text{O}}_4}=\text{RS}{{\text{O}}_4}+\text{Cu}$,故B正确;
C.由于金属活动性 $\text{R}>\text{H}$,所以 $\text{R}$ 能与 ${{\text{H}}_2}\text{S}{{\text{O}}_4}$ 反应,化学方程式 $\text{R}+{{\text{H}}_2}\text{S}{{\text{O}}_4}=\text{RS}{{\text{O}}_4}+{{\text{H}}_2}\uparrow $,故C正确;
D.由于金属活动性 $\text{Al}>\text{Zn}>\text{R}$,所以 $\text{Al}$ 能与 $\text{RS}{{\text{O}}_4}$ 反应,化学方程式 $\text{2Al}+3\text{RS}{{\text{O}}_4}=\text{Al}{{\left( \text{S}{{\text{O}}_4} \right)}_3}+3\text{R}$,故D正确;
故选A。
氢氧化钠与氢氧化钙是两种最常见的碱,下列有关它们的说法中正确的是()
氢氧化钠与氢氧化钙的溶液都呈碱性,都能使酚酞溶液变红色,选项A正确;
氢氧化钠具有吸水性,能用作干燥剂,氢氧化钙不能用作干燥剂,选项B不正确;
氢氧化钠溶液与二氧化碳反应无明显现象,不能用于检验二氧化碳气体,选项C不正确;
氢氧化钠具有虽腐蚀性,不能用作建筑材料,选项D不正确。
进行化学实验必须注意安全,下列做法不符合实际的是()
浓硫酸不慎沽到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液,氢氧化钠溶液具有强腐蚀性,故不能使用,选项D选项错误。
下列验证“ $\rm CO_2 $ 与 $\rm NaOH $ 溶液反应”的装置中,不能观察到明显现象的是(装置气密性均良好)( )
$\rm A$.通入二氧化碳时,虽然氢氧化钠能和二氧化碳反应生成生成碳酸钠和水,但是无明显现象;
$\rm B$.实验过程中,由于二氧化碳和氢氧化钠反应生成了碳酸钠和水,导致试管中气压减小,从而导致液体在试管中上升;
$\rm C$.实验过程中,由于二氧化碳和氢氧化钠反应生成了碳酸钠和水,导致气球膨胀;
$\rm D$.实验过程中,由于二氧化碳和氢氧化钠反应生成了碳酸钠和水,导致烧杯中的水流入锥形瓶中;
故选 $\rm A$。
下列实际应用中,利用中和反应原理的是( )
①用氢氧化钠溶液洗涤石油产品中的残余硫酸
②用碳酸氢钠治疗胃酸过多
③用熟石灰改良酸性土壤
④用稀氨水涂抹在蚊子叮咬处(分泌出蚁酸)止痒
①氢氧化钠与硫酸的反应为酸和碱的中和反应;
②碳酸氢钠是盐不是碱;
③熟石灰是碱能与酸性土壤发生中和反应;
④稀氨水显碱性,与酸反应生成可以消除蚊虫的叮咬,是中和反应;
故①③④正确;
故选D。
将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如图。由此分析下列说法不正确的是( )
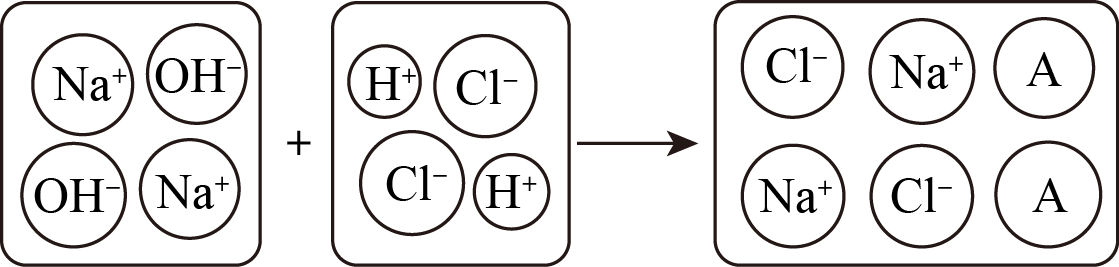
$\mathrm{NaOH}+\mathrm{HCl}=\mathrm{NaCl}+\mathrm{H}_{2} \mathrm{O}$
质量守恒定律
A.溶液在任何时间都是对外不显电性,所以正确;
B.反应前的溶质时氯化氢和氢氧化钠,反应后的溶质时氯化钠,根据质量守恒定律:$\mathrm{m}_{(\mathrm{NaOH})}+\mathrm{m}_{(H C 1)}=\mathrm{m}_{(\mathrm{NaCl})}+\mathrm{m}_{\left(\mathrm{H}_{2} \mathrm{O}\right)}$,所以反应后的溶质质量减少,所以错误;
C.恰好完全反应之后所得的溶液是氯化钠溶液,氯化钠溶液呈中性,所以正确;
D.反应后的溶液中的微观粒子有:$\mathrm{Na}^{+},\mathrm{Cl}^{-},\mathrm{H}_{2} \mathrm{O}$ ,所以A代表的是水分子,正确;
下列反应中属于中和反应的是( )
本题难度不大,掌握中和反应的特征(反应物是酸和碱,生成物是盐和水)是正确解答此类题的关键.
中和反应是指酸和碱作用生成盐和水的反应,判断中和反应时一要看反应物是否是酸和碱,二是看生成物是否是盐和水,二者缺一不可.
A、该反应的反应物是盐和酸,生成物是盐、水和二氧化碳,不属于中和反应,故A错误;
B、该反应是酸与碱反应生成盐和水的反应,属于中和反应,故B正确;
C、该反应的反应物是碱和非金属氧化物,不属于中和反应,故C错误;
D、该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故D错误.
故选:B.
类推是学习中常用的思维方法,现有以下类推结果,其中错误的是()
①碱的水溶液呈碱性,所以碱性溶液一定是碱的溶液 ;
②氧化物都含有氧元素,所以含氧元素的化合物定是氧化物;
③酸碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
碱性溶液不一定是碱的溶液,如碳酸钠溶液,①错误。
由两种元素组成,其中一种元素为氧元素的化合物为氧化物,②错误。
生成盐和水的反应不一定是中和反应,如氢氧化钠和二氧觉碳应生成碳酸钠(盐)和水,该反应不是中和反应,③错误。