如图所示,四圆分别表示浓溶液、稀溶液、饱和溶液、不饱和溶液的集合,A、B、C、D集合分别表示( )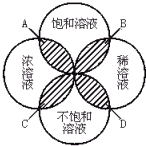
题目答案
您的答案
答案解析
分析:
饱和溶液和不饱和溶液的本质区别是:继续加入该溶质看能否溶解,和溶液的浓稀没有必然的关系.
解答:
解:从图中可以看出A处是饱和溶液和浓溶液的相交的区域,故A是饱和浓溶液;B是饱和溶液和稀溶液的相交处,B是饱和稀溶液;C是不饱和溶液和浓溶液的相交处,C是不饱和浓溶液,D处是不饱和溶液和浓溶液的相交的区域,故D是不饱和浓溶液;故答案:A.饱和浓溶液 B.饱和稀溶液 C.不饱和稀溶液 D.不饱和浓溶液,选A.
点评:
题考查的是有关浓、稀溶液与饱和溶液、不饱和溶液的关系,饱和溶液和不饱和溶液的转化,很好的锻炼了学生对溶液部分基础知识的掌握.