分析:
因为金属与酸反应时生成氢气的质量=$\frac {金属的化合价}{金属的相对原子质量}$×金属的质量,所以同质量的铝、镁与酸反应生成氢气的质量均大于铁,同理锌则小于铁而,铜与酸不反应,所以可以将铜的相对原子质量看成无限大.据此分析解答即可;
解答:
解:假设合金中铁的质量为5.6 g,则根据化学反应的方程式:Fe+2HCl=FeCl$_2$+H$_2$↑可计算出此时产生氢气的质量为0.2 g,同理可计算出5.6 gAl、镁与足量盐酸反应产生氢气的质量大于0.2 g,5.6gZn与足量盐酸反应产生氢气的质量小于0.2 g,
A、若混合物为Fe、Mg,氢气一定大于0.2g,故A错误;
B、若混合物为Fe、Zn,氢气一定小于0.2g,故B正确;
C、若混合物为含有铜,则氢气的质量一定小于0.2g,如果是生成0.1g氢气
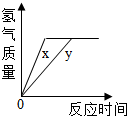
设参与反应的铁的质量是x
Fe+2HCl=FeCl$_2$+H$_2$↑
56 2
x 0.1g
$\frac {56}{2}$=$\frac {x}{0.1g}$
x=2.8g,故铁的质量分数为$\frac {2.8g}{5.6g}$×100%=50%,故C错误;
D、当粉末为Fe、Al合金时,因相同质量的铝消耗稀盐酸的质量比铁消耗盐酸的质量大;
设而5.6 g铁时,消耗盐酸的质量为y
Fe+2HCl=FeCl$_2$+H$_2$↑
56 73
5.6g y
$\frac {56}{5.6g}$=$\frac {73}{y}$
y=7.3g
此时盐酸的溶质质量分数为$\frac {7.3g}{100g}$100%=73%
所以合金为为Fe-Al合金时,所需盐酸溶质质量分数一定大于7.3%,故D正确;
故选BD
点评:
相同质量的金属与酸反应产生氢气的质量的多少与金属的相对原子质量和化合价有关.同价态的金属若相对原子质量越大,产生的氢气质量越小.