关于溶液的下列叙述中,正确的是( )
题目答案
您的答案
答案解析
A.溶液的概念:一种或几种物质分散到另一种物质里,形成均一、稳定的混合物叫溶液,可见溶液不一定只含有一种溶质,所以A错误;
B.一定温度下,一定量溶剂里溶解某种物质是有一定限度的,当不能继续溶解该物质时就得到该物质的饱和溶液,故B错误;
C.蔗糖溶液属于非电解质溶液,它不会导电,故C错误;
D.硝酸钾的溶解度随温度的升高而增大,升高温度,能加快溶解的速率,故D正确.
故选D
关于溶液的下列叙述中,正确的是( )
A.溶液的概念:一种或几种物质分散到另一种物质里,形成均一、稳定的混合物叫溶液,可见溶液不一定只含有一种溶质,所以A错误;
B.一定温度下,一定量溶剂里溶解某种物质是有一定限度的,当不能继续溶解该物质时就得到该物质的饱和溶液,故B错误;
C.蔗糖溶液属于非电解质溶液,它不会导电,故C错误;
D.硝酸钾的溶解度随温度的升高而增大,升高温度,能加快溶解的速率,故D正确.
故选D
下列有关溶液及其性质的说法错误的是()
海水中溶解的盐类物质使水的凝固点降低,选项A正确;
溶液中溶质以分子或离子的形式分散,而浊液中分散在液体中的物质颗粒较大,选项B正确;
在溶解度的概念中,溶剂的标准是 100 g,是一个定值,选项C错误;
食盐水中含有自由移动的离子,通电时,这些离子定向移动形成电流,选项D正确。
下列关于溶液的说法正确的是( )
溶液中溶剂只能有一种,溶质可以有多种;溶液中的溶质可以是固体液体或气体;无色透明的液体不一定是溶液,例如水是无色透明的液体,但水不是溶液;溶液的质量为溶质和溶剂质量之和。
下列各组物质混合形成的溶液中,前者是溶剂,后者是溶质的一组是( )
溶液中只要有水,水为溶剂,故A、B、D中溶剂均为水,即后者为溶剂;C中酒精为液体,作为溶剂,碘为固体,作为溶质;
故选C。
下列有关溶液的说法正确的是( )
下列各组物质中,前者是后者的溶质的是( )
如图为某盐酸试剂瓶上标签的部分内容。请仔细阅读后计算,欲配制 $14.6\%$ 的稀盐酸 $200\ \text{g}$,需要这种盐酸的质量为( )
盐酸(分析纯)
化学式:$\text{HCl}$ 相对分子质量:$36.5$
密度:$1.1\ \text{g/c}{{\text{m}}^3}$ 溶质质量分数:$20\%$ |
由于在用水稀释的过程中溶质的质量不变,则可设需浓溶液的质量为 $x$。
$x\times 20\%=200\rm \ g\times 14.6\%$,
$x=\frac{200\ \text{g}\times 14.6\%}{20\%}=146\ \text{g}$。
故选A。
2019年禽流感疫情仍在持续,相关药物主要是抗生素、板蓝根等。一种抗生素为粉末状固体,每瓶含0.5g,注射时应将其配成质量分数为20%的溶液,则使用时每瓶至少需加入蒸馏水()
根据题意可知,配制的溶液的质量=$\frac {溶质的质量} {溶质的质量分数 \}$=$\frac {0.5 g} {20 \%} = 2.5 g$,而所需溶剂的质量=溶液的质量-溶质的质量=2.5g-0.5g=2g,合2mL,故选选项B。
用氯化钠配制 $\rm 100 $ 克溶质质量分数为 $\rm 20\% $ 的氯化钠溶液,现有下列操作:①溶解,②称取氯化钠;③过滤;④量取水;⑤计算;⑥蒸发结晶,针对该实验说法正确的是( )
$\rm A$.固体溶质加水溶解的配制步骤为计算、称量、量取、溶解,所以本题答案为:⑤②④①;故 $\rm A$ 错误;
$\rm B$.配制 $\rm 100 $ 克溶质质量分数为 $\rm 20\% $ 的氯化钠溶液,所需氯化钠的质量为 $\rm 100~g~\times 20\% =20~g$,所需水的体积为 $\rm 80~mL$,所以需要选择 $\rm 100~mL$ 的量筒,故 $\rm B$ 正确;
$\rm C$.量筒是用来量取液体的体积,但不能用来配制溶液,故 $\rm C$ 错误;
$\rm D$.固体溶解度的概念是指一定温度下 $\rm 100~g$ 溶剂水中达到饱和状态所溶解的溶质的质量,该溶液不一定饱和,故 $\rm D$ 错误;
故选 $\rm B$。
配制 $10\%$ 的氯化钠溶液时,下列会引起溶液中溶质的质量分数偏小的是( )
使溶质质量分数偏小的情况有两种,一种是称取的氯化钠质量偏小,一种是加入的水过多。
A选项:量筒量取时俯视读数,会使实际称取的水的体积小于读数值,因此溶质质量分数偏大,故A错误;
B选项:配置溶液的烧杯用蒸馏水润洗,会使加入的水的质量增大,故溶质质量分数偏小,故B正确;
C选项:天平称量氯化钠时,指针左偏,说明称取氯化钠的质量大于理论值,故溶质质量分数偏大,故C错误;
D选项:溶液已经配好时,溶质质量分数已经确定。不会因为移液而使溶质质量分数发生变化,故D错误;
故选B。
小芳在配制一定溶质质量分数的氯化钠溶液时,没有按照正确的称量氯化钠。量取水的操作规程进行操作(图示为小芳操作时的读数,其它操作都正确)。小芳实际配制的氯化钠溶液的溶质质量分数(水的密度为 $1~\text{g}$/$\text{cm}^3$)约为( )
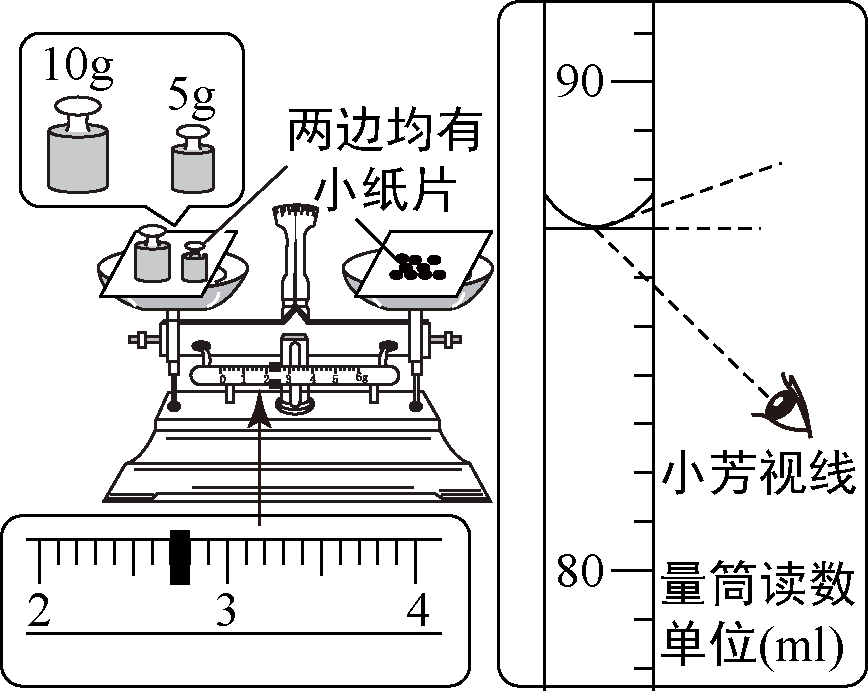
小芳用托盘天平称量时,将药品与砝码的位置放反了,使用的是 $10~\text{g}$ 和 $5~\text{g}$ 的砝码和 $2.7~\text{g}$ 的游码;由左盘的质量 $=$ 右盘的质量 $+$ 游码的质量可知:砝码质量 $=$ 药品质量 $+$ 游码的质量,所以药品质量 $=$ 砝码质量 $-$ 游码质量,即药品质量 $ = 10~\text{g} + 5~\text{g} - 2.7~\text{g} = 12.3~\text{g}$ 。
量取的水的实际体积为 $87~\text{mL}$ (合 $87~\text{g}$)。
小芳实际配制的氯化钠溶液的溶质质量分数为 $\frac{12.3~\text{g}}{12.3~\text{g}+87~\text{g}}\times 100\%\approx 12.4\%$ 。
故选A。