下列属于分解反应的是()
题目答案
您的答案
答案解析
问题要点
考查对分解反应的判断。常与其他化学基本反应类型结合在一起进行考查。解此类题时,抓住分解反应的特征“一变多”进行判断,即可轻松解答。
答案解析
选项1-中反应的反应物为一种,生成物为两种,符合分解反应“一变多”的特点,属于分解反应。
下列属于分解反应的是()
考查对分解反应的判断。常与其他化学基本反应类型结合在一起进行考查。解此类题时,抓住分解反应的特征“一变多”进行判断,即可轻松解答。
选项1-中反应的反应物为一种,生成物为两种,符合分解反应“一变多”的特点,属于分解反应。
化学概念间有包含、并列、交叉等不同关系。下列选项符合如图所示关系的是()
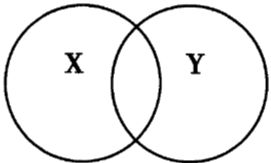
图中所示关系是交叉关系。化合反应中有的属于氧化反应,有的不属于氧化反应,氧化反应中有的属于化合反应,有的不属于化合反应,化合反应和氧化反应属于交叉关系;物质分为纯净物和混合物,所以混合物和纯净物是并列关系;物理变化和化学变化是并列关系;化合反应属于化学反应,二者是包含关系。
下列关于物质的性质和用途说法不正确的是( )
分析:
物质的性质决定物质的用途,物质具有多种性质,要理解物质的用途是由物质的哪种性质决定的,物质的化学性质是指在化学变化中表现出来的性质,物质的物理性质是指不需要通过化学变化表现出来的性质.
解答:
A、氧气具有助燃性,但是氧气不可燃,氧气被用作火箭的燃料,利用了氧气的助燃性,而不是可燃性,故A选项说法错误,故A符合题意;B、氮气常温下不活泼,氮气用来保护粮食,是利用氮气常温下化学性质稳的说法正确,故B不符合题意;C、稀有气体充入霓虹灯,是利用稀有气体通电能发出不同颜色的光的说法正确,故C不符合题意;D、二氧化碳不燃烧,也不支持燃烧,且密度比空气大,二氧化碳用于灭火,是利用它的物理性质和化学性质的说法正确,故D不符合题意;故选:A.
点评:
本题主要考查物质的性质和用途,物质具有多种性质,解答时应该理解物质的用途是由物质的哪种性质决定的.
日常生活中缓慢氧化的例子有很多,下列反应中不包含缓慢氧化的是()
物质与氧气的反应属于氧化反应,缓慢氧化是进行得非常缓慢、现象不易察觉的氧化反应。食物腐败、酒的酿造、动植物的呼吸都包含物质的缓慢氧化;酒精的燃烧进行迅速,现象明显,是较剧烈的氧化反应,故选选项3-。
物质的下列性质中,属于化学性质的是()
物质的性质可以分为物理性质和化学性质。物质在化学变化中表现出来的性质叫做化学性质,如物质的可燃性、氧化性、还原性、稳定性等都属于化学性质;物质不需要发生化学变化就表现出来的性质叫做物理性质,如物质的颜色、状态、气味、密度、硬度、熔点、沸点、溶解性、挥发性、导电性、导热性等都属于物理性质。物质的物理性质与化学性质的根本区别在于“是否需要通过化学变化才能表现出来”。
都是对物理性质、化学性质的描述和考查,判断的关键是看该性质是否需要通过化学变化才能表现出来和性质的具体内容。
判断物质的性质属于物理性质还是化学性质,关键是看该性质是否需要通过化学变化才能表现出来。不需要发生化学变化就表现出来的性质叫做物理性质;物质在化学变化中表现出来的性质叫做化学性质。可燃性需要经过燃烧才能表现出来,属于化学性质。
我国著名科学家张青莲教授主持测定了铕等9种元素的相对原子质量新值,已知铕原子的相对原子质量为152,核电荷数为63,则铕原子的核外电子为( )
分析:
根据“核内质子数=核外电子数=核电荷数”,由题意“铕原子的相对原子质量为152,核电荷数为63”,则可知铕原子的核外电子数.
解答:
解:根据“核内质子数=核外电子数=核电荷数”,由题意“铕原子的相对原子质量为152,核电荷数为63”,则可知铕原子的核外电子数为63.故选A.
点评:
了解原子的定义和构成:原子由原子核和核外电子构成,其中原子核由质子和中子构成的;熟记规律“原子序数=核内质子数=核外电子数=核电荷数”.
氧的相对原子质量为16,表示的意义是()
选项1-项,相对原子质量近似等于原子中质子数与中子数之和,所以氧原子的相对原子质量为16不能说明其原子核内质子数为16,错误;选项2-项,一个氧原子的质量远小于16g,错误;选项3-项,相对原子质量是一个原子的真实质量与一个碳12原子质量的$\frac {1} {12}$的比值,而不是一个碳原子质量的$\frac {1} {12}$,错误;选项4-项,一个氧原子的质量是一个碳12原子质量的$\frac {1} {12}$的16倍,正确。
图例为镁原子的结构示意图,下列所示粒子化学性质与其相似的是()
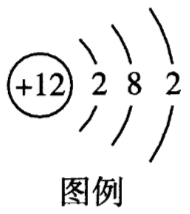
原子结构示意图中,圆圈内正数表示质子数(即核电荷数);弧线上的数字表示每一电子层上的电子数;弧线表示电子层,有几条弧线就表示有几个电子层。
介绍了原子结构示意图各部分的意义。考查结构示意图各部分的意义、应用及分子性质。解此类习题应首先明确结构示意图中各部分的含义,再根据质子数与电子数的相对大小关系判断该粒子属于原子、阳离子还是阴离子;决定原子种类的是质子数;应根据原子结构示意图中的最外层电子数判断原子的种类及化学性质:金属原子的最外层一般少于4个电子,易失去电子,非金属原子的最外层一般多于4个电子,易得到电子,而稀有气体原子的最外层为8(或2)个电子,化学性质相对稳定。一般情况下,原子最外层电子数相同,化学性质相似。要注意只有一个电子层的情况,如氦和镁最外层电子数都是2,但化学性质不相似。
原子中,最外层电子数相同,化学性质相似。镁原子最外层有2个电子,在化学反应中易失去2个电子。选项2-、选项4-中最外层都有2个电子,但选项2-只有一个电子层,第一层上有2个电子,已达到相对稳定结构,不易失去电子。
根据如图所示结构示意图提供的信息进行判断,下列说法中,
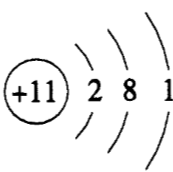
根据该粒子的结构示意图可知,该粒子原子核内有11个质子,最外层电子数为1,属于金属原子,易失去电子,该粒子核内质子数等于核外电子总数,呈电中性。
下列粒子结构示意图中,表示阳离子的是()
考查粒子的判断。判断某粒子是原子、阳离子还是阴离子时,一般根据质子数(核电荷数)与核外电子数的关系判断:质子数等于核外电子数的粒子是原子;质子数大于核外电子数的粒子是阳离子;质子数小于核外电子数的粒子是阴离子。
在粒子中,当质子数=核外电子数时,不显电性,为原子;当质子数>核外电子数时,带正电荷,为阳离子;当质子数<核外电子数时,带负电荷,为阴离子。
镉(Cd)被认为是一种十分危险的环境污染元素,长期摄入被镉严重污染的稻米、蔬菜、水果,饮用含镉量超标的水,都会出现镉慢性中毒的症状。元素符号“Cd”
元素符号既表示一种元素,又表示一个原子,但不一定都能表示某物质,只有由原子直接构成的物质,元素符号才能表示该物质。