在镁与稀硫酸的反应中,已知10s末硫酸的浓度减少了0.6mol/L,则10s内生成氢气的平均反应速率是( )
题目答案
您的答案
答案解析
分析:
先根据题意计算硫酸的反应速率,再根据同一反应中,各物质的反应速率之比等于其计量数之比计算氢气的平均反应速率.
解答:
点评:
本题考查的是反应速率的定量表示方法,侧重考查学生对化学反应速率的理解,知道同一反应中各物质的反应速率之比等于其计量数之比是解本题的关键.
在镁与稀硫酸的反应中,已知10s末硫酸的浓度减少了0.6mol/L,则10s内生成氢气的平均反应速率是( )
分析:
先根据题意计算硫酸的反应速率,再根据同一反应中,各物质的反应速率之比等于其计量数之比计算氢气的平均反应速率.
解答:
点评:
本题考查的是反应速率的定量表示方法,侧重考查学生对化学反应速率的理解,知道同一反应中各物质的反应速率之比等于其计量数之比是解本题的关键.
在2L密闭容器内,某气体反应物在2s内由8mol变为7.2mol,则用该物质表示反应的平均反应速率为( )
分析:
根据c=$\frac {$\frac {△n}{V}$}{△t}$计算2s内该物质表示的平均反应速率.
解答:
解:在2L密闭容器内,某气体反应物在2s内由8mol变为7.2mol,
2s内该物质表示的平均反应速率为$\frac {$\frac {8mol-7.2mol}{2L}$}{2s}$=0.2mol/(L•s),
故选C.
点评:
本题考查化学反应速率的有关计算,比较基础,注意对速率定义的理解利用.
在体积为2L的密闭容器中合成氨,已知在时间t内,氨的物质的量增加了0.6mol,在此时间内,用H$_2$表示的平均反应速率是0.45mol/(L•s),则t是( )
分析:
解答:
点评:
本题考查化学反应速率的有关公式,比较基础,注意速率公式的理解与灵活运用.
在反应3H$_2$+N$_2$⇌2NH$_3$ 中,经一段时间后,氨的浓度增加了0.6mol/L,在此时间内用H$_2$表示的平均反应速率为0.45mol/(L•s),则反应所经过的时间为( )
分析:
利用速率之比等于化学计量数之比计算出v(NH$_3$),再根据t=$\frac {△c}{v}$计算时间.
解答:
解:H$_2$ 表示的平均速率v(H$_2$ )=0.45mol/(L∙s),
利用速率之比等于化学计量数之比,所以v(NH$_3$)=$\frac {2}{3}$v(H$_2$ )=$\frac {2}{3}$×0.45mol/(L∙s)=0.3mol/(L∙s),
氨的浓度增加了0.6mol/L,即△c(NH$_3$)=0.6mol/L,
所以反应所经历的时间为$\frac {0.6mol/L}{0.3mol/(L.s)}$=2s,
故选:D.
点评:
本题考查化学反应速率的有关计算,难度不大,注意对公式的理解与灵活运用.
对A(g)+3B(g)⇌2C(g)来说,下列反应速率中最快的是( )
分析:
化学反应速率之比等于化学计量数之比,则反应速率与化学计量数的比值越大,反应越快,以此来解答.
解答:
解:反应速率与化学计量数的比值越大,反应越快,则
A.$\frac {0.3}{1}$=0.3,
B.$\frac {0.6}{3}$=0.2,
C.$\frac {0.5}{2}$=0.25,
D.$\frac {0.01×60}{1}$=0.6,
显然D中比值最大,反应最快,
故选D.
点评:
本题考查化学反应速率快慢的比较,为高频考点,把握比值法比较反应速率为解答的关键,侧重分析与计算能力的考查,注意单位要一致,题目难度不大.
某温度时,浓度都为1mol/L的两种气体X$_2$和Y$_2$,在密闭容器中反应生成气体Z,4s后X$_2$、Y$_2$、Z的浓度分别是0.4mol/L,0.8mol/L,0.4mol/L,如Z用X、Y表示,则该化学方程式可表示为( )
分析:
计算各物质的浓度变化量,利用浓度变化量之比等于化学计量数之比,据此确定各物质的化学计量数,再利用原子守恒用X、Y表示Z的组成,据此书写方程式.
解答:
解:4s后,△c(X$_2$)=1mol•L_-0.4mol•L_=0.6mol•L_,
△c(Y$_2$)=1mol•L_-0.8mol•L_=0.2mol•L_,
△c(Z)=0.4mol•L_,
则X$_2$、Y$_2$、Z的化学计量数之比为=0.6mol•L_:0.2mol•L_:0.4mol•L_=3:1:2,
故反应为3X$_2$+Y$_2$═2Z,根据原子守恒可知,Z为X$_3$Y,
故反应可以表示为:3X$_2$+Y$_2$═2X$_3$Y,
故选:C.
点评:
本题考查化学反应速率的有关计算,难度不大,根据物质的量浓度变化量之比等于化学计量数之比确定各物质的化学计量数是关键.
在2A+B⇌3C+5D反应中,表示该反应速率最快的是( )
分析:
根据化学反应速率之比等于化学计量数之比,把用不同物质表示的反应速率换算成用同一物质表示的化学反应速率,然后比较大小.
解答:
解:对反应2A+B=3C+5D,都换算成D表示的速率进行比较,
A、v(A)=0.5 mol/(L•s),速率之比等于化学计量数之比,故v(D)=$\frac {5}{2}$v(A)=$\frac {5}{2}$×0.5 mol/(L•s)=1.25 mol/(L•s);
B、v(B)=0.3mol/(L•s),速率之比等于化学计量数之比,故v(D)=5v(B)=5×0.5 mol/(L•s)=2.5 mol/(L•s);
C、v(C)=0.8 mol/(L•s),速率之比等于化学计量数之比,故v(D)=$\frac {5}{3}$v(C)=$\frac {5}{3}$×0.8 mol/(L•s)=1.33 mol/(L•s);
D、v(D)=1 mol/(L•s),
故B表示的反应速率最快,
故选B.
点评:
本题考查化学反应速率的比较,难度不大,注意转化为同一物质表示的速率,再进行比较,利用速率与对应化学计量数的比值判断更简单.
在四个不同的容器中进行合成氨的反应.根据下列在相同时间内测定的结果,判断生成氨的速率最快的是( )
分析:
同一化学反应中,同一时间段内,各物质的反应速率之比等于其计量数之比,先把不同物质的反应速率换算成同一物质的反应速率进行比较,从而确定选项,注意单位是否相同.
解答:
解:反应为N$_2$(g)+3H$_2$(g)⇌2NH$_3$(g),以氢气的反应速率为标准进行判断,
A.v(H$_2$)=0.3mol/(L•min);
B.v(N$_2$)=0.05mol/(L•s)=3mol/(L•min),反应速率之比等于其计量数之比,所以v(H$_2$)=9mol/(L•min);
C.v(N$_2$)=0.2mol/(L•min),反应速率之比等于其计量数之比,所以v(H$_2$)=0.6mol/(L•min);
D.v(NH$_3$)=0.3mol/(L•min),反应速率之比等于其计量数之比,所以v(H$_2$)=0.45mol/(L•min);
所以反应速率最快的是B.
故选:B.
点评:
本题考查了化学反应速率快慢的比较,难度不大,常用归一法与比值法判断,要注意单位是否相同.
对反应A+3B⇌2C+2D 来说,下列反应速率最快的是( )
分析:
由于不同物质表示的速率之比等于其化学计量数之比,故速率之比与其化学计量数的比值越大,表示的反应速率越快,据此解答.
解答:
解:A.$\frac {V_A}{1}$=0.15;
B.$\frac {V_B}{3}$=0.2;
C.$\frac {V_C}{2}$=0.2;
D.$\frac {V_D}{2}$=0.225,
故反应速率:V_D>V_B=V_C>V_A,
故选D.
点评:
本题考查化学反应速率比较,难度不大,注意理解速率规律,也可以利用归一法计算比较,但利用比值法更为简单,对于选择题更适用.
可逆反应A+3B⇌2C+2D,在四种不同的情况下的反应速率分别为:[br]①V_A=0.15 mol/(L•s) [br]②V_B=0.6 mol/(L•s) [br]③V_C=0.4 mol/(L•s) [br]④V_D=0.45 mol/(L•s)[br]该反应进行最快的是( )
分析:
利用比值法可知,反应速率与化学计量数的比值越大,则反应越快,以此来解答.
解答:
点评:
本题考查反应快慢的比较,注意利用比值法可快速比较反应的快慢,也可利用转化为同种物质的反应速率来比较快慢,注重基础知识的考查,题目难度不大.
关于如图所示实验装置的叙述错误的是( )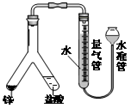
分析:
A.检查装置气密性原理通常是想办法造成装置不同部位有压强差,并产生某种明显现象,如气泡的生成,水柱生成,液面升降;
B.通过量气装置可测得产生氢气的体积,锌的质量可称量,锌的摩尔质量已知,则根据反应方程式可计算此条件下的气体摩尔体积;
C.根据氢气的体积得知锌的物质的量,锌的质量可称量,根据摩尔质量等于质量除以物质的量可求得锌的相对原子质量;
D.根据相似相溶原理作出判断.
解答:
解:A.由于此装置属于密闭体系,将水准管上提,造成内外压强不等,静置,若液面高于量气管且不下降,说明装置不漏气,故A正确;
B.通过量气装置可测得产生氢气的体积,锌的质量可称量,锌的摩尔质量已知,则根据反应方程式可计算此条件下的气体摩尔体积:Zn+2HCl═ZnCl$_2$+H$_2$↑
65 g/mol Vm
m g v L
Vm═65v/m L/mol,故B正确;
C.气体摩尔体积可当作已知,根据方程式同理可求得锌的摩尔质量,故C正确;
D.氢气为非极性分子,CCl$_4$为非极性分子,根据相似相溶原理,部分氢气溶在CCl$_4$中,造成测量误差,故D错误._故选D.
点评:
本题考察了仪器的创新实用.量气装置中所用液体一般是水,气体在水中溶解度很小;若气体在水中溶解度较大,可采用其他液体,比如四氯化碳等.