化学反应前后,各物质的质量总和之所以相等是因为( )
题目答案
您的答案
答案解析
分析:
化学反应的实质是分子分成原子,原子再重新组合成新的分子,化学反应前后原子的种类、数目、质量都不变.
解答:
解:由化学反应的实质是原子的重新组合,推出原子的种类、数目、质量都没有改变,所以化学反应前后各物质的质量总和必然相等.而物质种类、分子种类是一定改变
故选D
点评:
由化学反应的实质入手,因为原子是化学变化中的最小粒子,所以原子的种类、数目、质量都没有改变.
化学反应前后,各物质的质量总和之所以相等是因为( )
分析:
化学反应的实质是分子分成原子,原子再重新组合成新的分子,化学反应前后原子的种类、数目、质量都不变.
解答:
解:由化学反应的实质是原子的重新组合,推出原子的种类、数目、质量都没有改变,所以化学反应前后各物质的质量总和必然相等.而物质种类、分子种类是一定改变
故选D
点评:
由化学反应的实质入手,因为原子是化学变化中的最小粒子,所以原子的种类、数目、质量都没有改变.
在化学反应前后,下列粒子总数可能发生变化的是( )
分析:
化学反应的实质是分子分成原子,原子再重新组合成新的分子,所以反应前后分子的种类一定变,分子的数目可能变.化学反应前后宏观上反应前后物质总质量、元素的种类和微观上原子的种类、原子的数目、原子的质量不变.
解答:
解:化学反应的实质是:在化学变化中,分子分解成原子,原子重新组合成新的分子.在重新组合的过程中,原子的种类没有改变,原子的数目没有增减,原子的质量也没有变化.因此质子数、电子数也没有变化.但物质种类(分子种类)一定要改变,分子的数目可能改变,也可能不变.
故选D.
点评:
本题难度不大,掌握化学反应前后“五个不变”、“两个一定改变”、“两个可能改变”是正确解答本题的关键所在.
某反应的微观示意图如图,有关说法错误的是( )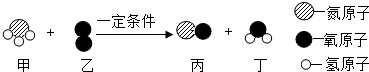
分析:
根据微观示意图分析反应物、生成物的分子构成,判断物质的化学式、类别,并写出反应的方程式,判断反应类型等.
解答:
解:观察四种分子的结构可知甲、乙、丙、丁分别是NH$_3$、O$_2$、NO、H$_2$O,根据化学反应前后原子的种类和个数都不变,因此反应的方程式为:4NH$_3$+5O$_2$$\xlongequal[]{一定条件}$4NO+6H$_2$O.
A、甲的一个分子由一个氮原子和三个氢原子构成的,因此化学式为:NH$_3$;故说法正确;
B、由反应的微观示意图及方程式可知,该反应的生成物是两种化合物,因此不属于置换反应,故说法错误;
C、丙和丁分别是NO、H$_2$O,都是氧化物,故说法正确;
D、根据微观示意图可知反应前后分子的种类发生了改变,故说法正确;
故选:B.
点评:
本题通过微观粒子的反应模型图,考查了微观上对化学反应的认识,学会通过微观示意图把宏观物质和微观粒子联系起来、从微观的角度分析物质的变化是正确解答此类题的关键.
某固体化合物R在加热条件下分解生成氧化铜,水,二氧化碳.取一定质量的R,加热一段时间后,下列说法正确的是( )
分析:
A、R属于纯净物,其中不含有二氧化碳和水;
B、反应前后,固体减少的质量等于生成二氧化碳的质量和生成水的质量之和;
C、R中铜元素的质量不一定等于生成氧化铜中铜元素的质量;
D、反应前后固体中的铜元素的质量不变,反应后固体的质量减小.
解答:
解:A、R中含有铜元素、氢元素、氧元素和碳元素,但是不含有二氧化碳和水,该选项说法不正确;
B、反应前后,固体减少的质量等于生成二氧化碳的质量和生成水的质量之和,该选项说法不正确;
C、如果R完全反应,则R中铜元素的质量一定等于生成氧化铜中铜元素的质量,如果R不完全反应,则R中铜元素的质量一定大于生成氧化铜中铜元素的质量,该选项说法不正确;
D、因为反应前后固体中的铜元素的质量不变,反应后固体的质量减小,所以反应后固体中铜元素的质量分数比反应前固体中铜元素的质量分数大,该选项说法正确.
故选:D.
点评:
解答时要注意,是加热一段时间后,没有说明是否完全反应,这是判断各个选项是否正确的关键.
临床试验证明,抗流感新药帕拉米韦(C$_1$5H$_2$8N$_4$O$_4$)注射液对流感有效.有关帕拉米韦的说法正确的是( )
分析:
A、根据帕拉米韦化学式的含义进行分析判断.
B、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
D、根据质量守恒定律:反应前后元素种类不变,进行分析判断.
解答:
解:A、帕拉米韦是由碳、氢、氮、氧四种元素组成的,故选项说法正确.
B、帕拉米韦的相对分子质量为12×15+1×28+14×4+16×4,故选项说法错误.
C、帕拉米韦中碳、氢元素的质量比为(12×15):(1×28)≠15:28,故选项说法错误.
D、由质量守恒定律:反应前后元素种类不变,帕拉米韦是由碳、氢、氮、氧四种元素组成,帕拉米韦在人体内反应后除生成二氧化碳和水外,还应生成含氮元素的物质,故选项说法错误.
故选A.
点评:
本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.
举世瞩目“神九”飞天会“天宫”.发射“神九”的长二F运载火箭使用的特种燃料含有液态偏二甲肼(化学式为C$_2$H$_8$N$_2$),下列关于偏二甲肼说法正确的是( )
分析:
A、根据偏二甲肼的微观构成进行分析判断.
B、根据偏二甲肼化学式的含义进行分析判断.
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
D、根据质量守恒定律进行分析判断.
解答:
解:A、偏二甲肼是由偏二甲肼分子构成的,偏二甲肼分子中含有氮原子,不含氮分子,故选项说法错误.
B、由偏二甲肼的化学式可知,偏二甲肼是由C、H、N三种元素组成,故选项说法正确.
C、该物质中C、H元素质量比为(12×2):(1×8)=3:1,故选项说法错误.
D、根据质量守恒定律,偏二甲肼完全燃烧产物除含有CO$_2$、H$_2$O,还应含有含氮元素的物质,故选项说法错误.
故选B.
点评:
本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算等进行分析问题、解决问题的能力.
AgNO$_3$固体见光或受热易分解,故用棕色试剂瓶保存.AgNO$_3$受热分解,放出的有刺激性气味的气体可能是( )
分析:
根据质量守恒定律:化学反应前后元素的种类不变,可初步的判断生成物是什么.然后根据题中放出有刺激性气味的气体可排除氮气;根据反应前AgNO$_3$中存在银、氮、氧三种元素,故反应后的生成物中不可能有SO$_2$和NH$_3$.
解答:
A、AgNO$_3$中不含有硫元素,根据质量守恒定律,不可能是SO$_2$,故A错误;
B、AgNO$_3$中存在银、氮、氧三种元素,NO$_2$又有刺激性气味,所以有可能,故B正确;
C、AgNO$_3$中不含有氢元素,根据质量守恒定律,不可能是NH$_3$,故C错误;
D、N$_2$无刺激性气味,不可能含有,故D错误;
故选B.
点评:
该题主要考查了质量守恒定律的应用,该题还要求学生要善于从题中挖掘出有用的解题信息(例如分解放出有刺激性气味的气体),以及要求学生要学会用排除法做选择题.
如图反映了某个化学反应各物质质量与时间的关系.下列描述正确的是( )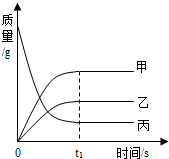
分析:
A、化合反应是指多种物质反应生成一种物质的反应,可以据此结合图象判断出反应物和生成物的种类,进行解答即可;
B、本题中不知道反应物和生成物的分子构成,所以难以判断相对分子质量的大小;
C、反应前后质量减少的为反应物,质量增加的为生成物,可以据此解答;
D、根据质量守恒定律的内容进行判断.
解答:
解:A、根据图象可以知道反应前后甲和乙的质量增加,故甲和乙为生成物,丙的质量减少,所以丙为反应物,不符合化合反应的特点“多变一”,故A错误;
B、本题中不知道反应物和生成物的分子构成,所以难以判断相对分子质量的大小,故B错误;
C、根据图象可以知道反应前后甲和乙的质量增加,故甲和乙为生成物,丙的质量减少,所以丙为反应物,故C正确;
D、根据质量守恒定律可以知道,参加反应的物质总质量等于反应后生成的物质的总质量,在t$_1$时,参加反应的丙的质量一定等于生成的甲、乙的质量之和,但是丙的质量不一定就等于甲乙的质量之和,因为此时丙还没有反应完全,故D错误.
故选C.
点评:
要想解答好这类题目,首先,要理解和熟记质量守恒定律及其应用,以及与之相关的知识.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.
在化学反应A+B=C+D中,已知80g A与24g B恰好完全反应生成42g C,则生成D的质量为( )
分析:
根据质量守恒定律:参加化学反应的各物质质量总和,等于反应后生成的各物质质量总和.
解答:
生成C的质量=80g+24g-42g=62g;
故选B.
点评:
回答本题应注意必须是参加反应的物质加在一块,没参加反应的不能加.
将20克甲、5克乙、8克丙三种纯净物混合,在密闭容器中加热发生化学反应,经分析可知:反应后混合物中含有5克甲、16克丙,还含有一种新物质丁.则丁物质的质量是( )
分析:
根据质量守恒定律,必须为参加化学反应前各物质的质量总和等于反应后生成各物质的质量总和;所以参加反应的B的质量可依据质量守恒定律来计算;则根据质量守恒定律,可求丁的质量.
解答:
方法一:因为“将20克甲、5克乙、8克丙三种纯净物混合,在密闭容器中加热发生化学反应,经分析可知:反应后混合物中含有5克甲、16克丙,还含有一种新物质丁”,则:甲的质量减少15克、乙的质量减少5克,二者为反应物;丙的质量增加8克,丁质量也增加,则二者为生成物,故根据质量守恒定律,可求丁的质量为:15+5-8=12克.
方法二:根据质量守恒定律,20克甲、5克乙、8克丙的总质量,等于反应后混合物中5克甲、16克丙,新物质丁的总质量.则丁物质的质量为20+5+8-(5+16)=12克.
故选A.
点评:
此题是质量守恒定律以及反应类型考查题,解题的关键是确定甲、乙、丙的质量,求丁的质量以及掌握反应类型的含义.
某纯净物M微热就能分解生成NH$_3$、H$_2$O和CO$_2$,由此还不能得出的结论是( )
分析:
根据题意“微热就能分解”,说明不稳定;“纯净物M微热就能分解生成NH$_3$、H$_2$O和CO$_2$”说明是化合物;“纯净物M”是不可能含有水的;根据质量守恒定律,由生成物可以推测反应物中的元素组成.
解答:
解:A、根据题意“微热就能分解”,说明不稳定;故A正确;
B、“纯净物M微热就能分解生成NH$_3$、H$_2$O和CO$_2$”,根据质量守恒定律:反应前后元素种类不变,则可知纯净物M含有多种元素,是化合物,故B正确;
C、“纯净物M”是不可能含有水的,故C错误;
D、根据质量守恒定律,由生成物可以推测反应物的元素组成,则M由氮、氢、碳、氧元素四种元素组成,故D正确.
故选:C.
点评:
根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和;掌握物质的元素组成;掌握单质和化合物的判别.