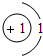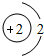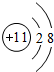分析:
根据RO$_2$为氧化物,相对分子质量是44,可以求出R的相对原子质量,
根据方程式中RO$_2$和N的质量比,以及RO$_2$的相对分子质量,可以求出N的相对分子质量.
再根据质量守恒定律,参加反应的各物质的质量总和应等于生成物的质量总和,此反应中参加反应的M和RO$_2$的质量和应等于生成物N的质量,由M和N的质量就可以求得RO$_2$的质量.
根据方程式中各物质的质量关系,可以判断2.4gM与5gR不会恰好完全反应,则生成N的质量小于7.4gN
解答:
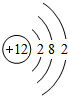
解:A、R的相对原子质量为:44-16×2=12,故A对
B、设N的相对分子质量为x
M+RO$_2$ $\xlongequal[]{高温}$ 2N
44 2x
4.4g 5.6g
$\frac {44}{2x}$=$\frac {4.4g}{5.6g}$
x=28
故B对.
C、参加反应的RO$_2$质量为:5.6g-1.2g=4.4g,故C错
D、设与2.4g M完全反应的 RO$_2$ 的质量为 y
M + RO$_2$ $\xlongequal[]{高温}$ 2N
1.2g 4.4g 5.6g
2.4g y
$\frac {1.2g}{4.4g}$=$\frac {2.4g}{y}$
y=8.8g
故RO$_2$不足,生成N的质量为$\frac {5g×5.6g}{4.4g}$≈6.36g. 故D错
故选C、D
点评:
解答此题要根据质量守恒定律和相对分子质量仔细分析,认真计算.