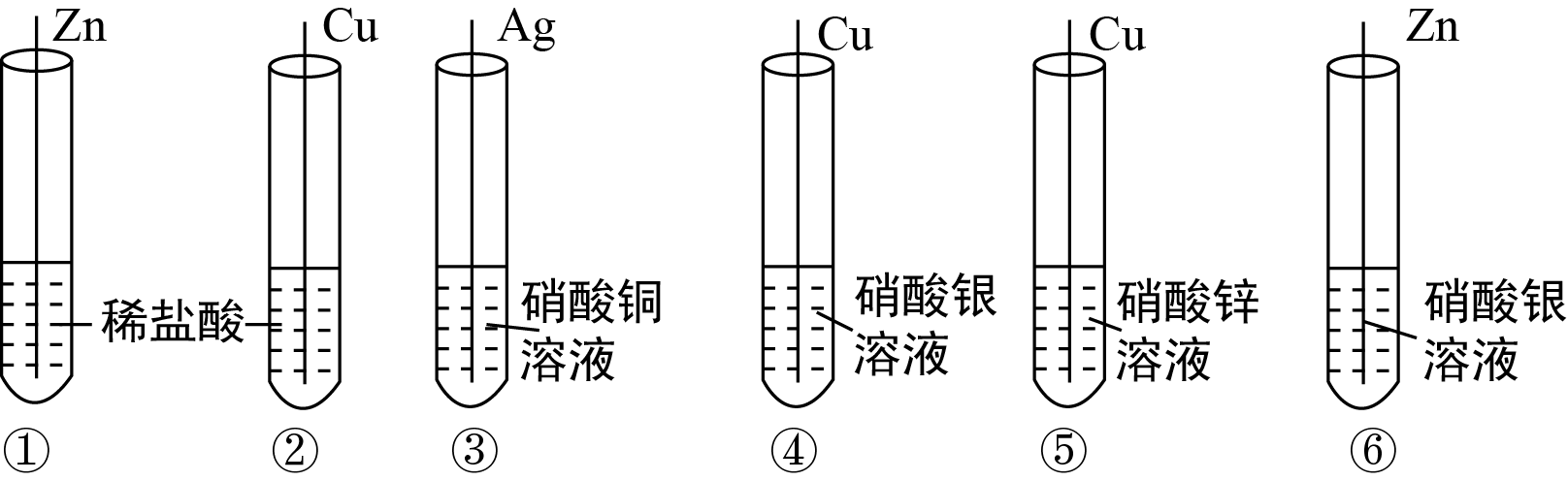
可可同学为验证锌、银、铜三种金属的活动性顺序,设计如图所示的六个实验,其中不能验证出三种金属的活动性顺序的组合是( )
题目答案
您的答案
答案解析
$\rm A$ 选项:①、②能验证锌比铜强,③能证明铜比银强,此项可验证三种金属的活动性顺序,故A错误;
$\rm B$ 选项:①、②能验证锌比铜强,④能证明铜比银强,此项可验证三种金属的活动性顺序,故B错误;
$\rm C$ 选项:③能证明铜比银强,⑤能验证锌比铜强,能验证三种金属的活动性,故C错误;
$\rm D$ 选项:①、②能验证锌比铜强,⑥能验证锌比银强,不能比较铜、银的强弱,不可验证三种金属的活动性顺序,故D正确;
故选 $\rm D$。

