用分子的知识解释下列现象,其中合理的是( )
题目答案
您的答案
答案解析
水结成冰,水分子仍在不断运动,选项1-项错误;变瘪的乒乓球放入热水中能鼓起来,是由于温度升高,分子间的间隔变大,分子本身体积不变,选项2-项错误;加入糖的水变甜,是由于分子永不停息地做无规则运动,选项3-项正确;大豆和小米是宏观物质,不能用微观粒子的性质解释,选项4-项错误。
用分子的知识解释下列现象,其中合理的是( )
水结成冰,水分子仍在不断运动,选项1-项错误;变瘪的乒乓球放入热水中能鼓起来,是由于温度升高,分子间的间隔变大,分子本身体积不变,选项2-项错误;加入糖的水变甜,是由于分子永不停息地做无规则运动,选项3-项正确;大豆和小米是宏观物质,不能用微观粒子的性质解释,选项4-项错误。
如图表示封闭在某容器中的少量液态水的微观示意图(该容器的活塞可以左右移动)。煮沸后,液态水变成水蒸气。在这一过程中,发生的变化是( )
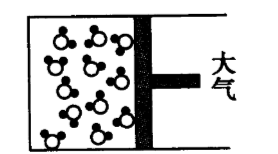
从微观角度分析,液态水变成水蒸气时,水分子之间的间隔变大,分子本身的体积、数目均没有变化。
下列关于分子和原子的说法中,错误的是( )
选项A,分子、原子都是构成物质的微粒,正确;选项B,由分子构成的物质,分子是保持其化学性质的最小粒子,正确;选项C,在化学变化中,分子分成原子,原子再重新结合成新的分子,原子是化学变化中的最小粒子,正确;选项D,分子和原子之间都有间隔,对于不同的物质,分子之间的间隔不一定比原子之间的间隔大,错误。
下列各图中,“•”和“○”分别表示两种不同元素的原子,其中表示混合物的是( )
选项1-图中表示了一种分子,该分子含有两种原子,该物质由一种分子构成,属于纯净物;选项2-图中表示了三种分子,属于混合物;选项3-图中表示了一种分子,该分子含有一种原子,该物质由一种分子构成,属于纯净物;选项4-图中表示了一种分子,该分子含有一种原子,该物质由一种分子构成,属于纯净物。
科学家用单个分子制成了“纳米车”(如图),它能在人工操纵下运输药物分子到病源处释放以杀死癌细胞。下列有关“纳米车”的说法正确的是( )
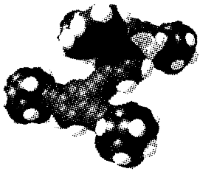
由题意可知,随着科技的发展,在一定条件下可以人为控制分子的运动。“纳米车”是由单个分子制成的,质量、体积均很小,用肉眼看不见。
要善于从化学的视角认识世界。对下列事实的解释错误的是( )
选项1-项,人能闻到花香是因为分子在不断地运动,正确;选项2-项,水和酒精混合之后体积小于二者体积之和是因为两者分子间有间隔,混合后微粒之间相互穿插渗透,正确;选项3-项,水变成水蒸气是物质的三态变化,属于物理变化,分子之间间隔变大,但分子本身大小不变,错误;选项4-项,氮气、氧气的化学性质不同是因为物质不同,即分子性质不同,正确。
卢瑟福的α粒子轰击金箔实验推翻了汤姆森在1903年提出的原子结构模型,为建立现代原子理论打下了基础。图线条中,可能是粒子(带正电)在该实验中的运动轨迹的是( )
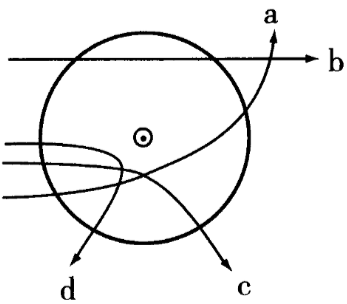
原子核和α粒子都带正电荷,同种电荷相互排斥,α粒子不可能偏向原子核,则运动轨迹a不正确,b、c、d都有可能。
学习完“原子的构成”之后,萍萍同学形成了以下认识,其中错误的是( )
原子由原子核和核外电子构成,故选项A说法正确;核外电子是分层排布的,电子在离核远近不同的区域中运动,故选项B说法正确;电子的质量很小,可以忽略不计,原子的质量主要集中在原子核上,故选项C说法错误;原子核的体积很小,与整个原子的体积相比要小得多,故选项D说法正确。
下表列出了几种原子中的粒子数。
原子种类 | 质子数 | 中子数 | 核外电子数 |
氢 | 1 | 0 | 1 |
碳 | 6 | 6 | 6 |
氧 | 8 | 8 | 8 |
钾 | 19 | 20 | 19 |
氢碳氧钾
分析上表中信息,下列说法正确的是( )
分析表中信息:原子核内质子数与中子数不一定相等;原子核内可以没有中子,如氢原子;原子一般是由质子、中子和电子构成的;原子中质子数与核外电子数相等。
原子的构成示意图如图,下列叙述正确的是( )
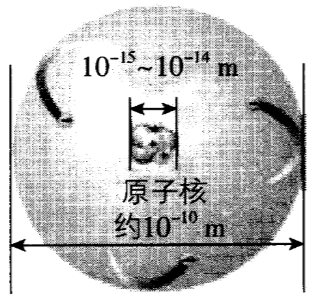
原子是由居于中心带正电的原子核和核外电子构成的,所以原子不是一个实心球体,故选项1-错误;原子核是由质子和中子构成的,电子的质量很小,每个电子的质量大约是每个质子质量的11836,所以原子的质量主要集中在原子核上,故选项2-正确,选项3-错误;质子、中子构成的原子核居于中心,电子在核外围绕原子核做高速运转,所以三者并不是均匀分布在原子中,故选项4-错误。故选选项2-。
下列关于原子核的叙述中,正确的是( )
①通常由中子和电子构成
②通常由质子和中子构成
③带负电荷
④不显电性
⑤不能再分
⑥体积大约相当于原子
⑦质量大约相当于原子
原子核是由质子和中子构成的,质子带正电,中子不带电,所以原子核带正电荷,原子核的体积只占整个原子体积的几万分之一,因为电子的质量很小,所以整个原子的质量主要集中在原子核上,决定原子质量大小的粒子是质子和中子。故选选项2-。