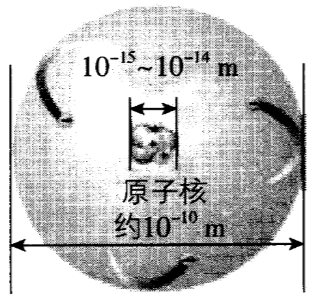
原子的构成示意图如图,下列叙述正确的是( )
题目答案
您的答案
答案解析
原子是由居于中心带正电的原子核和核外电子构成的,所以原子不是一个实心球体,故选项1-错误;原子核是由质子和中子构成的,电子的质量很小,每个电子的质量大约是每个质子质量的11836,所以原子的质量主要集中在原子核上,故选项2-正确,选项3-错误;质子、中子构成的原子核居于中心,电子在核外围绕原子核做高速运转,所以三者并不是均匀分布在原子中,故选项4-错误。故选选项2-。
原子的构成示意图如图,下列叙述正确的是( )

原子是由居于中心带正电的原子核和核外电子构成的,所以原子不是一个实心球体,故选项1-错误;原子核是由质子和中子构成的,电子的质量很小,每个电子的质量大约是每个质子质量的11836,所以原子的质量主要集中在原子核上,故选项2-正确,选项3-错误;质子、中子构成的原子核居于中心,电子在核外围绕原子核做高速运转,所以三者并不是均匀分布在原子中,故选项4-错误。故选选项2-。
下列关于原子核的叙述中,正确的是( )
①通常由中子和电子构成
②通常由质子和中子构成
③带负电荷
④不显电性
⑤不能再分
⑥体积大约相当于原子
⑦质量大约相当于原子
原子核是由质子和中子构成的,质子带正电,中子不带电,所以原子核带正电荷,原子核的体积只占整个原子体积的几万分之一,因为电子的质量很小,所以整个原子的质量主要集中在原子核上,决定原子质量大小的粒子是质子和中子。故选选项2-。
对以下四种粒子的结构示意图,分析错误的是( )
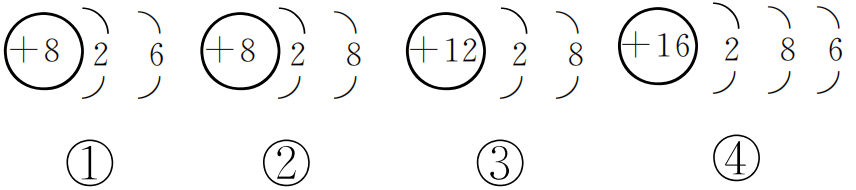
②③的最外层电子数都为 8,化学性质都比较稳定;①④最外层电子数相同,故两者化学性质相似;①③的质子数不同,①得到电子不可能形成③;②③的质子数不同,核内质子数都不等于核外电子数,表示不同种离子。
根据如图所示结构示意图提供的信息进行判断,下列说法中,
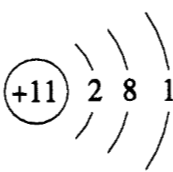
根据该粒子的结构示意图可知,该粒子原子核内有11个质子,最外层电子数为1,属于金属原子,易失去电子,该粒子核内质子数等于核外电子总数,呈电中性。
图例为镁原子的结构示意图,下列所示粒子化学性质与其相似的是( )
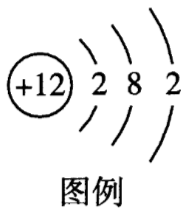
原子结构示意图中,圆圈内正数表示质子数(即核电荷数);弧线上的数字表示每一电子层上的电子数;弧线表示电子层,有几条弧线就表示有几个电子层。
介绍了原子结构示意图各部分的意义。考查结构示意图各部分的意义、应用及分子性质。解此类习题应首先明确结构示意图中各部分的含义,再根据质子数与电子数的相对大小关系判断该粒子属于原子、阳离子还是阴离子;决定原子种类的是质子数;应根据原子结构示意图中的最外层电子数判断原子的种类及化学性质:金属原子的最外层一般少于4个电子,易失去电子,非金属原子的最外层一般多于4个电子,易得到电子,而稀有气体原子的最外层为8(或2)个电子,化学性质相对稳定。一般情况下,原子最外层电子数相同,化学性质相似。要注意只有一个电子层的情况,如氦和镁最外层电子数都是2,但化学性质不相似。
原子中,最外层电子数相同,化学性质相似。镁原子最外层有2个电子,在化学反应中易失去2个电子。选项2-、选项4-中最外层都有2个电子,但选项2-只有一个电子层,第一层上有2个电子,已达到相对稳定结构,不易失去电子。
我国著名科学家、中国科学院院士张青莲教授主持测定了铟、铱、锑、铕等几种原子的相对原子质量新值,其中测定核电荷数为63的铕原子的相对原子质量的新值为152。则下列说法正确的是( )
铕原子的核电荷数为63,则其质子数为63,核外电子数也为63;相对原子质量为152,则中子数=152-63=89;相对原子质量不是原子的实际质量,152为铕原子的相对质量而非实际质量。
一个重水分子是由两个重氢原子和一个氧原子构成的,重氢原子的核电荷数是1,相对原子质量是2,则下列说法中正确的是( )
原子中,核电荷数=质子数=核外电子数,重氢原子的核电荷数为1,则重氢原子核外有1个电子,故选项1-项说法错误;重氢原子核内有1个质子,故选项2-项说法正确;重氢原子的相对原子质量是2,相对原子质量近似等于原子中质子数与中子数之和,则核内中子数为2−1=1,故选项3-项说法错误;虽然重分子和水分子中氧原子的相对原子质量相同,但由于重氢原子和氢原子中的中子数不同,因此重氢原子和氢原子的相对原子质量不同,故重水分子和水分子的相对分子质量不同,故选项4-说法错误。
1991年,我国著名化学家张青莲教授与另一位科学家合作,测定了铟(In)元素的相对原子质量的新值。铟元素的核电荷数为49,相对原子质量为115。铟原子的核外电子数为( )
原子中,质子数=核电荷数=核外电子数,铟原子的核电荷数为49,则其核外电子数也为49,故选项4-正确。
下列有关元素和原子的叙述中正确的是( )
元素是宏观概念,只论种类不论个数,原子是微观概念,既论种类又论个数,故选项1-正确;在化学反应中,分子可分而原子不可再分,故选项2-错误;氯化氢是由氯元素和氢元素组成的,元素只论种类不论个数,故选项3-错误;一种元素最少含有一种原子,可能含有多种原子,故原子的种类比元素的种类要多,故选项4-错误。
如图是甲、乙两种微粒的结构示意图,下列有关说法正确的是( )
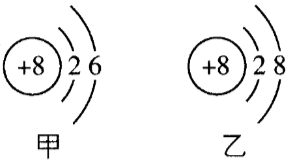
选项1-项,元素的种类由质子数决定,甲、乙的质子数都为8,故属于同种元素,正确;选项2-项,相对原子质量≈质子数+中子数,故甲微粒的相对原子质量应大于8,错误;选项3-项,乙微粒的质子数为8,小于其核外电子数(10),故是一种阴离子,错误;选项4-项,乙微粒最外层电子数为8,达到稳定结构,故乙微粒比甲微粒稳定,错误。
水是生命之源,既普通又宝贵.下列对水的“多”与“少”的描述错误的是( )
A、生活中接触的水大多是水的溶液,所以接触的纯水少,水溶液多,故A错误;B、我国水资源总量多,人均水量少,故B正确;C、在我国南方水多,北方水少,故C正确;D、地球上水的总量多,但是大多是海水,淡水少,故D正确.故选A.