某温度时,A物质的溶解度是25g,则A的饱和溶液中溶质的质量分数是()
题目答案
您的答案
答案解析
饱和溶液中溶质的质量分数= 溶解度 溶解度 +100g×100%。某温度时,A物质的溶解度是25g,则A的饱和溶液中溶质的质量分数是25g25g+100g×100%=20%。
某温度时,A物质的溶解度是25g,则A的饱和溶液中溶质的质量分数是()
饱和溶液中溶质的质量分数= 溶解度 溶解度 +100g×100%。某温度时,A物质的溶解度是25g,则A的饱和溶液中溶质的质量分数是25g25g+100g×100%=20%。
将10g溶质质量分数为10%的氯化钠溶液变为20%,下列操作正确的是( )
设加入氯化钠的质量为x,根据题意有10g×10%+x10g+x×100%=20%,解得x=1.25g,选项A错误;
设蒸发水的质量为y,10 g×10%10g−y×100%=20%,解得y=5g,选项B正确;
由于溶液具有均一性,倒出一半溶液,剩余溶液的质量分数仍为10%,选项C错误;
将10g溶质质量分数为20%的氯化钠溶液加入10g溶质质量分数为10%的氯化钠溶液中,混合后溶液的浓度小于20%,选项D错误。
泡菜具有独特的风味,适合制作泡菜的食盐水浓度是4%.在配制4%的食盐水时,会导致溶液浓度偏小的是( )
①称量好的食盐倒入烧杯时,有少许洒出
②量水的体积时,俯视量筒
③溶解食盐的烧杯内壁是潮湿的
④用4g食盐和100g水配制溶液.
分析:
溶质氯化钠质量偏小或溶剂水的体积偏大,是导致配制氯化钠溶液时溶质质量分数偏小即溶液中NaCl质量分数小于4%的原因.
解答:
①称量好的食盐倒入烧杯时,有少许洒出导致溶解氯化钠质量偏小,所配制氯化钠溶液的质量分数偏小;②用量筒量取水时俯视读数,读数大于所量水的实际体积,使量取水的体积偏小,所配制氯化钠溶液的质量分数偏大;③溶解食盐的烧杯内壁是潮湿的,水的体积因此而偏大,所配制氯化钠溶液的质量分数偏小;④用4g食盐和100g水配制溶液溶质的质量分数是:4g100g+4g×100%=3.8%,所配制氯化钠溶液的质量分数偏小.答案:B.
点评:
抓住导致配制溶液时所出现误差的根本原因:溶质量或多或少、溶剂量或多或少,分析操作对溶质、溶剂量所造成的影响,使此类问题可以轻松解决.
实验室用氯化钠固体配制100g溶质质量分数为8%的氯化钠溶液,下列说法中错误的是()
配制100g溶质质量分数为8%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,选项A说法正确。
配制100g溶质质量分数为8%的氯化钠溶液,需氯化钠的质量为100gx8%=8g,需水的质量为100g-8g=92g(合92mL),应用规格为100mL的量筒量取水,选项B说法正确。
用量筒量取水时,俯视液面,会造成实际量取的水的体积偏小,使溶质质量分数偏大,选项C说法错误。
溶解过程中玻璃棒搅拌的作用是加快氯化钠的溶解速率,选项D说法正确。
将浓盐酸稀释为10%的盐酸时,不需要使用的仪器是()
将浓盐酸稀释为10%的盐酸时,实验步骤是计算、量取、混匀。用量筒与胶头滴管准确量取浓盐酸和水,用烧杯和玻璃棒完成混匀。
用氯化钠固体配制200g溶质质量分数为10%的氯化钠溶液,不需要涉及的步骤是()
配制一定溶质质量分数的溶液的步骤为计算、称量量取、溶解,不包含结晶操作,故选项D符合题意。
实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏小的是()
①称量的氯化钠固体中含有不溶性杂质;
②用量筒量取水时仰视读数;
③往烧杯中加水时有水酒出;
④将配制好的溶液装入试剂瓶中时有少量溅出。
①称量的氯化钠固体中含有不溶性杂质,会造成实际称取的溶质的质量偏小,使溶质质量分数偏小;②用量筒量取水时们视读数,读数比实际液体体积小,会造成实际量取的水的体积偏大,使溶质质量分数偏小;③往烧杯中加水时有水酒出,会造成溶剂水的质量偏小,使溶质质量分数偏大;④将配制好的溶液装入试剂瓶中时有少量溅出,溶液具有均一性,溶质质量分数不变。故①②操作会导致结果偏小。
实验室要配制50g溶质质量分数为5%的NaCl溶液,下列说法正确的是()
配制50g溶质质量分数为5%的NaCI溶液,需氯化钠的质量为50g×5%=2.5g,需水的质量是50g−2.5g=47.5g(合47.5mL),选项1-错误;天平指针向右偏转,说明药品质量小于砝码质量,应继续向左盘添加氯化钠,直至天平平衡,选项2-错误;量筒读数时,视线要与量筒内凹液面的最低处保持水平,选项3-正确;标签上应填写溶液的名称、溶质的质量分数,图中应填写氯化钠溶液5%,不需要标注溶液质量,选项4-错误。
下列关于空气的说法正确的是()
选项1-项,空气中氮气的体积分数为78%,错误;选项2-项,通常情况下,空气中氧气、氮气的体积比约为1∶4,正确;选项3-项,二氧化碳是植物光合作用不可缺少的物质,错误;选项4-项,稀有气体在空气中的体积分数是0.94%,不是含量最少的气体,错误。
图为空气成分示意图(按体积分数计算),其中“a”代表的是()
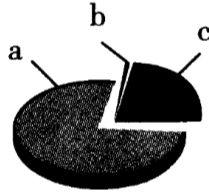
考查空气的成分,考查的难度不大,只需记住空气中各种成分的含量和空气中各种成分的性质即可。
空气的成分按体积计算,大约是:氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%、其他气体和杂质0.03%。根据图示可知,a占的体积分数最大,为氮气。
用如图所示装置进行实验。下列现象能证明空气中O2含量的是()
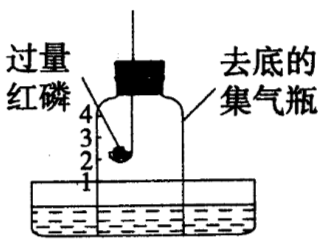
红磷燃烧产生大量的白烟,待红磷熄灭,冷却后打开弹簧夹,烧杯中的水沿导管进入集气瓶内,进入集气瓶内水的体积约占集气瓶内空气总体积的1/5。说明空气中氧气约占空气总体积的1/5。
利用红磷的燃烧来探究空气中氧气的含量,考查空气中氧气含量测定的相关知识。此类题无论采用哪种装置,其原理是相同的,即选择一种在空气中反应只消耗氧气而不与其他气体反应且生成物几乎不占气体空间的物质(如固体),使密闭容器中气体减少(减少的气体体积即为氧气的体积)。
红磷与氧气反应生成固体五氧化二磷,产生白烟,只能证明空气中有氧气,不能证明氧气的含量,选项1-错误;瓶中液面先下降,后上升,说明瓶内压强先变大后变小,无法证明氧气的含量,选项2-错误;将瓶内体积分成五等份,足量的红磷耗尽了装置内的氧气,冷却至室温后,瓶内的水面上升至刻度1处,说明瓶内气体减少了五分之一,证明氧气约占空气体积的五分之ー,选项3-正确;水槽内液面下降,只能说明瓶内压强变小,不能证明氧气的含量,选项4-错误。