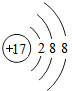
下列粒子结构示意图中,表示阳离子是( )
题目答案
您的答案
答案解析
分析:
根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;据此进行分析解答.
解答:
解:A、质子数=8,核外电子数=10,质子数<核外电子数,为阴离子,故选项错误.
B、质子数=核外电子数=10,为原子,故选项错误.
C、质子数=12,核外电子数=10,质子数>核外电子数,为阳离子,故选项正确.
D、质子数=9,核外电子数=10,质子数<核外电子数,为阴离子,故选项错误.
故选:C.
点评:
本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.
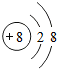
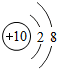
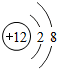
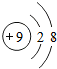
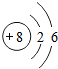
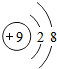
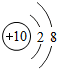
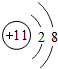

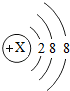 ,则X=( )
,则X=( )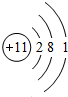 ,不能确定的是( )
,不能确定的是( )