某元素的原子核外有三个电子层,其电子数依次为2、8、4,则该元素是( )
题目答案
您的答案
答案解析
分析:
根据核外电子排布确定其原子序数及元素在周期表中的位置,进而确定元素.
解答:
解:元素的原子核外有三个电子层,其电子数依次为2、8、4,处于周期表中第三周期ⅣA族,原子序数为14,故为Si元素,故选C.
点评:
本题考查结构与位置关系,比较基础,注意对基础知识的理解掌握.
某元素的原子核外有三个电子层,其电子数依次为2、8、4,则该元素是( )
分析:
根据核外电子排布确定其原子序数及元素在周期表中的位置,进而确定元素.
解答:
解:元素的原子核外有三个电子层,其电子数依次为2、8、4,处于周期表中第三周期ⅣA族,原子序数为14,故为Si元素,故选C.
点评:
本题考查结构与位置关系,比较基础,注意对基础知识的理解掌握.
某元素的原子核外有三个电子层,最外层电子数是核外电子数的 $\frac {1}{6}$,该元素的元素符号是( )
分析:
根据核外电子排布规律推出某元素的原子结构示意图,根据原子序数等于核内质子数求得元素的种类.
解答:
解:因某元素的原子核外有三个电子层,设原子第三个电子层电子数为x,每一层上的电子数分别为:2、8、x,最外层电子数是核外电子数的 $\frac {1}{6}$,则:$\frac {1}{6}$(2+8+x)=x,解得x=2,
所以该原子序数为12,镁元素,元素符号为Mg,
故答案为:Mg,所以选C.
点评:
本题考查元素的推断和元素的性质,难度不大,熟悉核外电子排布是解决本题的关键.
核外电子分层排布的主要原因是( )
分析:
核外电子分层排布的主要原因是电子的能量不同,在原子核外能量低的排在离核近的区域,而能量高的电子排在离核远的区域.
解答:
解:A、电子的能量不同,按照能量的高低在核外排布,故A正确;
B、对于某一原子来说其电子的大小相同,不能根据其大小来排布,故B错误;
C、电子的数量不同时仍然是按照电子的能量高低来分层排布的,故C错误;
D、电子的质量很小,对某一原子来说,每个电子的质量是相同的,故D错误.
故选A.
点评:
学生应正确理解微观粒子的性质,具有空间想象的能力,明确电子的能量不同是分层排布的主要原因.
下列有关原子核外电子的说法错误的是( )
分析:
A.电子在核外作无规则高速运动;B.电子在原子中处于不同的能级状态,按能量不同分层排布;C.K层为最外层时最多可容纳2个电子;D.原子核外区域能量不同,距核由近到远,能量由低到高.
解答:
解:A.原子核外的电子,在核外不停的作无规则高速运动,故A正确;B.电子在原子中处于不同的能级状态,按能量不同分层排布,即电子在核外是分层排布的,故B正确;C.K层为最外层时最多可容纳2个电子,其它电子层作最外层时最多可容纳8个电子,故C错误;D.原子核外区域能量不同,距核由近到远,能量由低到高,即离原子核近的电子能量低,离原子核远的电子能量高,故D正确.故选C.
点评:
本题考查了核外电子的运动和电子排布规律,题目难度不大,易错选项是C,注意每个电子层作为最外层时,最多可容纳8个电子,但第一电子层除外,第一电子层最多排2个电子..
最外层电子数决定( )
分析:
根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,决定元素化学性质的是最外层电子数进行分析判断.
解答:
解:元素的化学性质跟它的原子的最外层电子数目关系非常密切,决定元素化学性质的是最外层电子数.
A、最外层电子数决定元素的化学性质,而不是决定原子量,故选项错误.
B、最外层电子数决定元素的化学性质,而不是决定中子数,故选项错误.
C、最外层电子数决定元素的化学性质,而不是决定质子数,故选项错误.
D、最外层电子数决定元素的化学性质,故选项正确.
故选D.
点评:
本题难度不大,掌握决定元素化学性质的是最外层电子数是正确解答本题的关键.
下列原子结构示意图代表的粒子属于金属元素的是( )
分析:
原子结构示意图中,若原子的最外层电子数为8,则为稀有气体元素,属于相对稳定结构;若最外层电子数≥4,则一般为非金属元素,在化学反应中易得电子,若最外层电子数<4,则一般为金属元素,在化学反应中易失去电子.
解答:
解:A、最外层电子数是5,大于4,为非金属元素,在化学反应中易得到3个电子而形成阴离子,故选项错误.
B、最外层电子数是1,小于4,为金属元素,在化学反应中易失去1个电子而形成阳子,故选项正确.
C、最外层电子数是6,大于4,为非金属元素,在化学反应中易得到2个电子而形成阴离子,故选项错误.
D、最外层电子数是7,大于4,为非金属元素,在化学反应中易得到1个电子而形成阴离子,故选项错误.
故选B.
点评:
本题难度不大,考查学生对原子结构示意图及其意义的理解,了解原子结构示意图的意义是正确解题的关键.
氟原子的结构示意图为: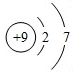 ,下列说法错误的是( )
,下列说法错误的是( )
分析:
根据原子结构示意图的意义分析,圆圈内的数字表示质子数,圆圈外的弧线表示电子层,电子层上的数字表示电子层上的电子数,根据最外层上的电子数分析元素的性质.
解答:
解:A、由氟原子的结构示意图可知,氟原子的核内质子数为9,故A正确;
B、由氟原子的结构示意图可知,氟原子核外有2个电子层,故B正确;
C、由氟原子形成的氟气分子是双原子分子,化学式是F$_2$,故C正确;
D、由氟原子的结构示意图可知;最外层电子数是7,在化学反应中,氟元素的一个原子容易得到1个电子形成阴离子,故D错误.
故选D.
点评:
本题难度不大,掌握原子结构示意图中各部分的含义及核外电子在化学反应中的作用是解题的关键.
下列四种粒子的结构示意图中,属于金属元素原子的是( )
分析:
因为:金属元素的原子最外层电子数一般为<4;非金属元素的原子最外层电子数一般≥4;稀有气体的元素的原子(氦为2)最外层电子数为8,所以可推测答案.
解答:
A、该粒子最外层电子数为2,所以为金属元素原子,故A正确;
B、该粒子最外层电子数为8,且质子数等于核外电子数,故为稀有气体元素原子,故B不符合题意;
C、该粒子最外层电子数为8,但质子数小于核外电子数,故为阴离子,为氧离子,故C不符合题意;
D、该粒子最外层电子数为7,所以为非金属元素原子,故D不符合题意.
故选A.
点评:
了解元素的简单分类;了解原子结构示意图与离子结构示意图的特点.
下列具有相似化学性质的是( )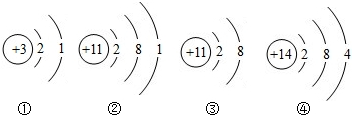
分析:
根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似;进行解答.(先根据当核电荷数=质子数=核外电子数,为原子;判断出原子的微粒;再解答)
解答:
根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,可得
A、①②的结构为原子,最外层电子数相同,化学性质相似;故A正确;
B、②为原子结构,③为离子结构,化学性质跟它的原子的最外层电子数目关系非常密切,故B错误;
C、②④都为原子结构,最外层电子数不相同;故C错误;
D、③为离子结构,④为原子结构,化学性质跟它的原子的最外层电子数目关系非常密切;故D错误;
故选A.
点评:
本题考查学生对最外层电子数相同的元素化学性质相似的前提是原子结构,理解与掌握及在解题中的应用.
如图所示是某原子结构示意图,有关它的说法错误的是( )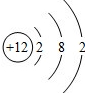
分析:
根据:原子序数=核电荷数=核外电子数=核内质子数,已知某原子结构示意图,可知它为镁原子.
解答:
A、圆圈内的数字就为质子数,则核内有12个质子,故A正确;
B、已推测它为镁元素,则为金属元素,故B错误;
C、由原子结构示意图,可知它有3个电子层,故C正确;
D、它的最外层电子数为2,说法正确,故D正确.
故选B.
点评:
了解原子结构示意图与离子结构示意图的区别和联系;掌握核外电子在化学变化中的作用和得失电子的规律特点.
如图为某原子的结构示意图,该原子的原子核中有( )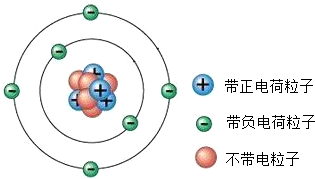
分析:
在原子中,质子数=核外电子数,原子核是由带正电的质子和不带电的中子构成的.
解答:
解:因为原子中,6个质子数=核外电子数,由该原子的结构示意图可知,其原子核外有6个电子,所以原子核内有6个质子,原子核是由质子和中子构成的,故选A.
点评:
本题考查了原子核的构成,明确原子核是由质子和中子构成的,在原子中,质子数=核外电子数是解题的关键.