将一根洁净的铁钉放人稀硫酸中,下列预测可能不正确的是( )
题目答案
您的答案
答案解析
铁能与稀硫酸反应生成硫酸亚铁与氢气,所以铁钉表面将产生气泡,溶液由无色变为浅绿色;由于溶解的铁的质量大于生成氢气的质量,所以溶液质量将增加;铁钉表面不会出现铁锈。
将一根洁净的铁钉放人稀硫酸中,下列预测可能不正确的是( )
铁能与稀硫酸反应生成硫酸亚铁与氢气,所以铁钉表面将产生气泡,溶液由无色变为浅绿色;由于溶解的铁的质量大于生成氢气的质量,所以溶液质量将增加;铁钉表面不会出现铁锈。
如图所示的四个图像,分别对应四种过程,其中正确的是( )
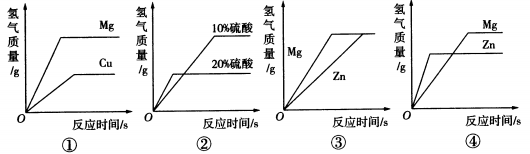
Cu不能与稀硫酸反应,与稀硫酸混合不会产生氢气,A错误;等质量、不同浓度的稀硫酸,浓度大的稀硫酸所含的氢元素质量大,等质量的稀硫酸与等质量且足量的Zn反应时,酸完全反应,所以稀硫酸浓度越大产生的氢气越多,B错误;等质量、等浓度的稀硫酸与等质量且足量的Mg、Zn反应,产生氢气的质量相等,且Mg比Zn活泼,反应速率快,C正确;等质量的Mg和Zn与等质量、等浓度且足量的稀硫酸反应,Mg产生的氢气比Zn多,且Mg比Zn活泼,反应速率快,D错误。

相同质量的$Mg、Fe、Zn$三种金属,分别与足量的、质量相同、质量分数相同的稀$H _ {2} SO _ {4}$充分反应,生成氢气与消耗稀$H _ {2} SO _ {4}$的质量关系如图。分析图像所得的结论中,不正确的是()
图像的横坐标为稀硫酸质量,由图中信息不能判断三种金属的活动性顺序,故选项1-错误;三种金属和稀硫酸反应生成的硫酸盐中金属元素的化合价都是﹢2,因为参加反应的三种金属的质量相同,所以生成氢气质量越小,金属的相对原子质量越大,由图中信息可知,生成氢气质量由小到大的顺序是锌、铁、镁,因此三种金属的相对原子质量:$Mg<Fe<Zn$,故选项2-正确;生成氧气质量越大,消耗稀硫酸质量越大,因此三种金属消耗稀$H _ {2} SO _ {4}$的质量:$Mg>Fe>Zn$,故选项3-正确;由题意可知,加入稀硫酸的质量相等,参加反应的三种金属的质量相同,则生成氢气质量越大,反应后形成溶液的质量越小,因此三种金属与稀$H _ {2} SO _ {4}$反应后溶液的质量:$Mg<Fe<Zn $,故选项4-正确。
相同质量的$Mg$、$Fe$分别与稀盐酸反应,产生氢气的质量$m(H _ {2})$与加人稀盐酸的体积$V$(稀盐酸)关系如下所示,其中正确的是( )
(1)等质量金属与足量的酸反应

图8-2-1
图8-2-1图反映出:
①金属越活泼,曲线越陡。
②当金属在化合物中化合价相同时,金属的相对原子质量越小,与酸反应产生的氢气越多,曲线的拐点越高。
(2)足量的金属与等量的酸反应
金属是足量的,说明酸完全反应,最终生成氢气的质量相等。如图8-2-2:

图8-2-2
$Mg$和$Fe$都能和盐酸反应,当酸过量,相同质量的两种金属完全反应时,$Mg$和稀盐酸反应得到的氢气质量多;当参加反应的酸不足时,生成的氢气质量应该相等,所以图像选项D正确。
下列物质中,能由金属跟盐酸直接反应制取的是()
铁与盐酸反应的产物为氯化亚铁;不是氯化铁,选项A错误;
银不能置换出盐酸中的氢,无法生成$AgCl$,选项B错误;
锌能与盐酸反应生成氯化锌,选项C正确;
铜不能置换出盐酸中的氢,无法生成$CuCl _ {2}$,选项D错误。
苹果、梨等多种水果的细胞中都含有輮酸。鞣酸能和铁反应,生成黑色的鞣酸铁与氢气,所以苹果、梨用铁刀切开以后,表面会变黑。下列四种金属中,能与鞣酸反应生成氢气的是()
金属活动性顺序中,排在氢前面的金属,能与酸反应生成氢气,四种金属中只有锌能与酸反应生成氢气。
两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加人稀硫酸的质量关系如图所示。下列说法正确的是()
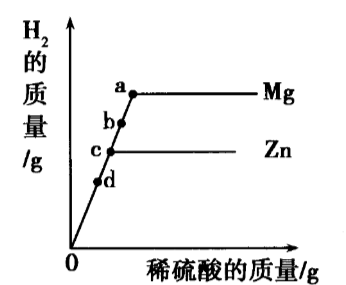
a点时,镁与稀硫酸恰好完全反应,锌早已完全反应:b点时,镁与稀硫酸反应产生的氢气多,锌与稀硫酸反应产生的氢气少;c点时,锌与稀硫酸恰好完全反应,镁有剩余;d点时,锌与镁均还没有完全反应,两个烧杯中都有金属剩余。
将质量相等的镁粉和铁粉分别投入等质量等浓度的稀硫酸中,所得 ${{\text{H}}_2}$ 质量与稀硫酸质量关系曲线正确的是( )
反应的稀硫酸质量相等时,生成氢气质量也相等,最终镁和稀硫酸反应生成的氢气多,$\rm B$ 对应关系正确;
故选 $\rm B$。
下列关于置换反应说法正确的是( )
$\rm A$.$\rm Cu$ 是金属活动顺序表中氢后金属,所以 $\rm Cu$ 不会与酸发生置换反应,但是可以与排在铜后面的银的盐溶液发生置换反应,故 $\rm A$ 错误;
$\rm B$.碳酸盐与酸也会反应产生气体,故 $\rm B$ 错误;
$\rm C$.硝酸是强氧化性酸,不能与金属发生置换反应,故 $\rm C$ 错误;
$\rm D$.置换反应中有单质参加和生成,故一定发生元素化合价的改变,故 $\rm D$ 正确;
故选 $\rm D$。
关于置换反应说法一定正确的是( )
A.置换反应不一定在溶液中进行,如碳还原氧化铜,故A错误
B.置换反应发生时,一定有元素化合价的改变,故B正确
C.有单质和化合物生成不一定是置换反应,如一氧化碳还原氧化铁,故C错误
D.如铁丝的燃烧,存在形式发生改变,但不是置换反应,故D错误
置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,据此分析。
金属材料的使用影响着人类的生活质量。用活泼金属制取不活泼金属是常用的方法,如$4 Na + TiCl _ {4} \stackrel {\text {高温}} {=}$$4 NaCl + Ti$,该化学反应的基本反应类型是()
该反应是一种单质与一种化合物反应生成另一种单质和另一种化合物,属于置换反应。