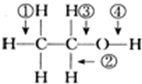
(多选)医生在给病人注射前,往往要用蘸有酒精的棉球在皮肤的相应部位进行擦抹,擦抹后患者往往感到相应部位有一种清凉的感觉,下面有关说法中不正确的是( )
题目答案
您的答案
答案解析
分析:
A、乙醇可以使蛋白质变性;
B、酒精具有挥发性,据此解答即可;
C、医用酒精的浓度通常是75%,此浓度杀菌消毒作用强;
D、碘酒能用于杀菌消毒,碘易于刺激皮肤灼伤.
解答:
解:A、乙醇能使蛋白质变性,故常用于病人的注射消毒,故A正确;
B、酒精具有挥发性,能用于人工降温,故B正确;
C、医用酒精的浓度通常是75%,此浓度杀菌消毒作用强,不是纯酒精,故C错误;
D、碘酒可用于伤口的消毒,碘易于刺激皮肤灼伤,所以不宜用碘酒代替此种酒精用于此类操作,故D错误;
故选CD.
点评:
本题主要考查的是酒精的物理性质以及生活中的常见应用,掌握乙醇的性质是解决本题的关键,难度不大.