- 第六章 金属
- 6.1 金属材料的物理特性
- 金属的物理性质
- 神奇的合金特性
- 6.2 金属的化学性质
- 金属的化学性质
- 金属活动性顺序
- 置换反应
- 6.3 金属矿物与冶炼
- 几种金属矿物
- 钢铁是怎样炼成的
- 不纯的化学方程式的计算
- 6.4 珍惜和保护金属资源
- 钢铁锈蚀
- 金属保护
- 第七章 溶液
- 7.1 溶解与乳化
- 溶解
- 乳化现象
- 溶解时的吸热或放热现象
- 7.2 物质溶解的量
- 饱和溶液与不饱和溶液
- 固体物质的溶解度
- 固体物质溶解度的表示方法
- 气体物质的溶解度
- 7.3 溶液浓稀的表示
- 溶液的浓度
- 溶质质量分数的简单计算
- 配制一定溶质质量分数的溶液
- 7.4 结晶现象
- 晶体与结晶
- 混合物的分离
- 第八章 常见的酸、碱、盐
- 8.1 溶液的酸碱性
- 区分酸碱性溶液和碱性溶液
- 检验溶液酸碱性强弱的程度
- 8.2 常见的酸和碱
- 常见的酸
- 稀酸的化学性质
- 常见的碱
- 碱溶液的化学性质
- 8.3 酸和碱的反应
- 酸和碱的组成
- 中和反应
- 中和反应的应用
- 酸雨的形成及危害
- 8.4 常见的盐
- 几种常见的盐的用途
- 盐的组成和化学性质
- 复分解反应发生的条件
- 8.5 化学肥料
- 常用化肥
- 铵态氮肥的检验
- 防止化肥施用对环境的污染
- 第九章 现代生活与化学
- 9.1 有机物的常识
- 有机物的特征
- 几种简单的有机物
- 9.2 化学合成材料
- 常见有机合成材料
- “白色污染”的危害与治理
- 9.3 化学能的利用
- 9.4 化学物质与健康
- 人体内的元素
- 食物中的营养素
科粤版初三下学期化学
《盐的组成和化学性质》考点精粹
盐的概念
1.盐
(1)盐的概念:组成里含有金属离子(或铵根离子)和酸根离子的化合物。
(2)生活中常见的盐:氯化钠、硫酸铜、碳酸钙、碳酸钠、碳酸氢钠、高锰酸钾等。
说明:
盐的分类:①根据盐所含阳离子的不同,盐可分为钾盐、钠盐、铵盐等;②根据盐所含酸根离子的不同,盐可分为硝酸盐、盐酸盐、碳酸盐等。
盐的化学性质
(1)盐的溶解性
钾盐、钠盐、铵盐、硝酸盐仝部可溶;盐酸盐除$AgCl$外全部可溶;硫酸盐除$BaSO _ {4}、PbSO _ {4}$不溶,$CaSO _ {4}、Ag _ {2} SO _ {4}$微溶外均可溶;碳酸盐除$Na _ {2} CO _ {3}、K _ {2} CO _ {3}、( NH _ {4} ) _ {2} CO _ {3}$可溶,$Mg CO _ {3}$微溶外均不可溶。
(2)盐的化学性质
在一定条件下,盐能与金属、酸、碱以及另一种盐发生反应,见下表:
性质 | 反应发生的条件 | 实例 |
盐+金属→新盐+新金属 | ①盐要溶于水; ②金属的活动性强于盐溶液中金属的活动性 | $Fe + CuSO _ {4} = Cu + FeSO _ {4}$ $Cu + 2 AgNO _ {3} =2 Ag + Cu ( NO _ {3} ) _ {2}$ |
盐+酸→新盐+新酸 | ①酸必须是可溶性的; ②符合复分解反应发生的条件 | $AgNO _ {3} + HCl = AgCl \downarrow + HNO _ {3}$ $\left. \begin{array} {l} {CaCO _ {3} + 2 HCl = CaCl _ {2} +} \\ {CO _ {2} \uparrow + H _ {2} O} \end{array} \right.$ |
盐+碱→新盐+新碱 | ①反应物都能溶于水; ②符合复分解反应发生的条件 | $\left. \begin{array} {l} {Na _ {2} CO _ {3} + Ca ( OH ) _ {2} =} \\ {CaCO _ {3} \downarrow + 2 NaOH} \end{array} \right.$ $\left. \begin{array} {l} {Na _ {2} CO _ {3} + Ba ( OH ) _ {2} =} \\ {BaCO _ {3} \downarrow + 2 NaOH} \end{array} \right.$ |
盐+盐→新盐1+新盐2 | ①反应物都能溶于水; ②符合复分解反应发生的条件 | $NaCl + AgNO _ {3} = AgCl \downarrow + NaNO _ {3}$ $CuSO _ {4} + BaCl _ {2} = BaSO _ {4} \downarrow + CuCl _ {2}$ |
巧学妙记盐的化学性质
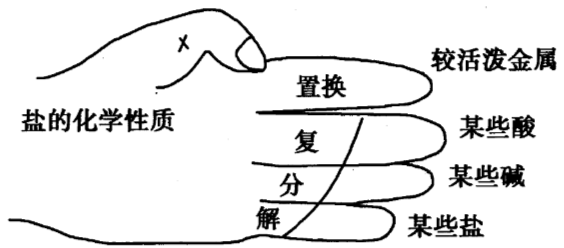
盐的组成和化学性质