- 第八单元 金属和金属材料
- 课题1 金属材料
- 几种重要的金属
- 合金
- 课题2 金属的化学性质
- 金属与氧气的反应
- 金属与盐酸、稀硫酸的反应
- 置换反应
- 金属与其他金属化合物溶液的反应
- 金属活动性顺序
- 课题3 金属资源的利用和保护
- 金属资源的存在形式及常见的矿石
- 铁的冶炼
- 有关化学反应中杂质问题的计算
- 金属资源保护
- 实验活动4 金属的物理性质和某些化学性质
- 第九单元 溶液
- 课题1 溶液的形成
- 溶液
- 溶解时的吸热或放热现象
- 乳化现象
- 课题2 溶解度
- 饱和溶液
- 固体溶解度
- 气体溶解度
- 课题3 溶液的浓度
- 溶质质量分数
- 溶液的计算
- 溶液的配制
- 实验活动5 一定溶质质量分数的氯化钠溶液的配制
- 第十单元 酸和碱
- 课题1 常见的酸和碱
- 酸、碱与指示剂作用
- 常见的酸
- 常见的碱
- 课题2 酸和碱的中和反应
- 中和反应
- 中和反应在实际中的应用
- 溶液酸碱度的表示法——pH
- 了解溶液酸碱性的重要意义
- 实验活动6 酸、碱的化学性质
- 实验活动7 溶液酸碱性的检验
- 第十一单元 盐 化肥
- 课题1 生活中常见的盐
- 氯化钠
- 粗盐提纯
- 碳酸钠、碳酸氢钠和碳酸钙
- 复分解反应
- 盐的化学性质
- 课题2 化学肥料
- 常见化肥的种类和作用
- 使用化肥、农药与环境的关系
- 化肥的简易鉴别
- 实验活动8 粗盐中难溶性杂质的去除
- 第十二单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
《固体溶解度》考点精粹
固体溶解度
1.定义:
在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂中的溶解度。若不指明溶剂,通常所说的溶解度是指物质在水里的溶解度。
2.固体溶解度概念中的四要素
溶解度四个要素 | 解释 |
条件: 在一定温度下 | 物质的溶解度会随温度的变化而变化 |
标准:在100g溶剂里 | 此处100g指溶剂质量,而不是指溶液质量 |
状态:饱和 | 规定只有在一定量溶剂中达到饱和状态时,所溶解的溶质的量才是一个确定的值 |
单位:克 | 溶解度实质上是溶解溶质的最大质量 |
3.溶解度的含义
①已知某物质在一定温度下的溶解度,其含义是指该物质在该温度下,在100g溶剂里达到饱和状态时所溶解的质量。
②通过溶解度可得到该温度下的该物质的饱和溶液中,溶质、溶剂和饱和溶液之间的质量关系,即溶质、溶剂和饱和溶液二者质量比为:溶解度:100g:(100g+溶解度)。
4.影响固体物质溶解度的因素
①内部因素:溶质和溶剂本身的性质。
②外部因素:温度。
5.固体物质溶解度与溶解性的关系
溶解性:只是定性地说明某种物质在某种溶剂里溶解能力的大小,是物质的一种物理性质。
根据物质溶解性的不同可以把物质分为易溶物质、可溶物质、微溶物质、难溶物质。
20℃时固体物质溶解度大小与溶解性的关系如下表。
溶解度 /g(20℃) | <0.01 | 0.01-1 | 1 -10 | >10 |
溶解性分类 | 难溶 | 微溶 | 可溶 | 易溶 |
举例 | $AgCl$、 $CaCO_{3}$ | $Ca(OH)_{2}$ | $KClO_{3}$ | $KNO_{3}$、 $NaCl$ |
溶解度曲线
1.定义
用纵坐标表示溶解度,横坐标表示温度,得到物质的溶解度随温度变化的曲线,这种曲线叫溶解度曲线。
2.溶解度曲线的变化规律
①陡升型:大多数固体物质的溶解度随温度升高而增大,表现在曲线“坡度”上升且比较“陡”,如$KNO_{3}$。
②缓升型:少数固体物质的溶解度受温度变化的影响很小,表现在曲线“坡度”比较“平缓”,如$NaCl$。
③下降型:极少数固体物质的溶解度随温度的升高而减小,表现在曲线“坡度”下降,如$Ca(OH)_{2}$。
3.溶解度曲线的意义
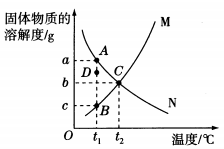
内容 | 意义 | |
点 | 曲线上的点 | 表示该物质在对应温度时的溶解度 |
两曲线的交点 | 表示两物质在对应温度时的溶解度相等 | |
线 | (1)表示物质在不同温度下的溶解度 (2)表示物质的溶解度随温度变化的趋势 | |
面 | 曲线下面的点 | 表示溶液是对应温度下该物质的不饱和溶液 |
曲线上面的点 | 表示溶液饱和且有未溶解的固体 | |
4.溶解度曲线的应用
①查出某种物质在某温度时的溶解度。
②可以看出物质的溶解度随温度变化的规律。
③比较不同物质在同一温度时的溶解度大小。
④可以比较不同物质的溶解度受温度变化影响的大小。
⑤根据溶解度曲线确定如何制得某温度时的该物质的饱和溶液。
⑥由溶解度曲线可确定从溶液中析出晶体的最佳方法。