- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 参观实验室
- 练习实验基本操作
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第四章 生命之源--水
- 4.1 我们的水资源
- 爱护水资源
- 水的净化和纯化
- 硬水及其软化
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第三章 维持生命之气--氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 催化剂
- 氧气的制取
- 分解反应
- 3.3 燃烧条件与灭火原理
- 燃烧与灭火
- 爆炸与防爆安全
- 3.4 物质组成的表示式
- 化学式和化合价
- 和化学式有关的计算
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 空气中有哪些成分
- 氮气和稀有气体有用吗
- 纯净物和混合物
- 保护空气
- 2.2 构成物质的微粒(1)--分子
- 2.3 构成物质的微粒(2)--原子和离子
- 原子
- 离子
- 2.4 辨别物质的元素组成
- 什么是元素
- 元素名称和符号
- 单质和化合物
- 元素周期表
- 第五章 燃料
- 5.1 洁净的燃料--氢气
- 5.2 组成燃料的主要元素--碳
- 碳有哪些单质
- 碳燃烧生成什么
- 5.3 二氧化碳的性质和制法
- 二氧化碳的性质
- 二氧化碳的制备
- 二氧化碳对人类生活的影响与碳循环
- 5.4 古生物的“遗产”--化石燃料
- 学生实验活动记录和报告
- 实验一 化学实验简单的基本操作
- 药品的取用
- 酒精灯的使用
- 玻璃仪器的洗涤
- 实验二 氧气实验室制取、性质与物质燃烧的条件
- 过氧化氢制取氧气
- 高锰酸钾制取氧气
- 实验三 二氧化碳实验室制取与性质
《实验三 二氧化碳实验室制取与性质》实验全解
实验目的
1.练习实验室里制取二氧化碳和用向上排空气法收集气体。
2.加深对二氧化碳性质的认识。
实验用品
烧杯、集气瓶、量筒、玻璃导管、胶皮管、单孔橡胶塞、铁架台(带铁夹试管、试管夹、玻璃片、酒精灯。
大理石(或石灰石)稀盐酸(1:2)澄清石灰水、紫色石蕊溶液、蜡烛、木条、蒸馏水、火柴。
实验装置
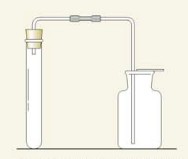
图(a)

图(b)

图(c)
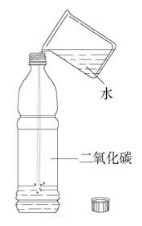
图(d)
实验步骤
1.制取二氧化碳
(1)实验准备:根据实验要求,清点实验仪器和药品。
(2)连接仪器,检查装置的气密性。
①玻璃管与胶皮管连接:左手拿胶皮管,右手拿直角导管,用水湿润玻璃管口,稍稍用力将玻璃管插入胶皮管。
②玻璃管与橡胶塞连接:将玻璃管口用水湿润,对准橡胶塞上的孔稍用力转动,将其插入,导管稍露出橡胶塞即可。
③容器口塞橡胶塞:将橡胶塞慢慢转动着塞进容器口。
④检查图(a)气密性方法:将导管浸入水中,手紧握试管外壁,导管口有气泡冒出,说明气密性良好。
(3)装药品:先装固体,后装液体。
①取盛大理石的试剂瓶,将瓶塞取下倒放在桌面上。
②取镊子,用干净的纸擦拭几次,然后取几块大理石。
③将试管横放,将大理石放在试管口,然后慢慢将试管直立起来,让大理石滑到试管底部。
④取下盛稀盐酸的瓶塞,倒入适量稀盐酸。
⑤左手拿试管,右手拿带导管的单孔橡胶塞,慢慢转动塞入试管口。
⑥将试管固定在铁架台上,试管底部触及铁架台台面,不要悬空。
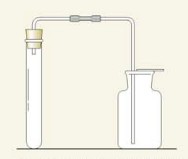
(4)收集二氧化碳:将导管伸入集气瓶底部,瓶口盖上玻璃片,用向上排空气法收集。
(5)验满:将燃着的木条放在集气瓶口,木条熄灭,证明已收集满。
2.二氧化碳的性质
(1)验证二氧化碳密度比空气大,不燃烧、不支持燃烧。
①把一支短蜡烛固定在烧杯内,点燃。
②拿起收集满二氧化碳的集气瓶,向烧杯内缓慢倾倒CO2,如图(b)所示。

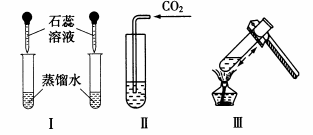
(2)验证CO2能与水反应
①取两支试管分别加入蒸馏水。
②向两支试管中分别滴入1~2滴石蕊溶液,振荡。
③将其中一支试管放在试管架上,向另一支试管中通入二氧化碳观察到试管内液体变红后停止通二氧化碳,并
与静置的试管中溶液颜色对比。
④将通入二氧化碳的试管放在酒精灯火焰上加热,观察现象。
实验现象:图(c)中紫色石蕊溶液变成红色,Ⅲ中溶液由红色又变成紫色。
(3)验证二氧化碳与石灰水反应。
①取一支试管倒入少量澄清石灰水,倾倒时标签向着手心,取下瓶塞倒放,瓶口紧挨试管口缓缓倾倒,倾倒1
~2mL后刮一下,盖上瓶塞,标签朝外放回原处。
②通入二氧化碳,观察到明显现象后停止通入。
实验现象:澄清石灰水变浑浊。
通入二氧化碳至看到石灰水变浑浊后就停止通入,若继续通入,石灰水又会变澄清,其原因是二氧化碳和碳酸
钙在水中又生成易溶于水的碳酸氢钙。
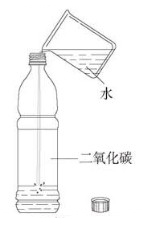
(4)验证CO2能溶于水
①收集一软塑料瓶CO2
②向塑料瓶中倒入约三体积的水,立即盖紧瓶塞振荡,观察现象。
实验现象:塑料瓶变瘪。
实验结论
(1)CO2密度大于空气,并且CO2不燃烧不支持燃烧。
(2)CO2和水发生了反应:$ H_ {2}O + CO_ {2} \stackrel {} {=} H_ {2}CO_ {3} $ ,碳酸具有酸性,能
够使湿润的紫色石蕊变红。
(3)CO2能使澄清石灰水变浑浊:$ Ca(OH)_ {2} + CO_{2} \stackrel {} {=} CaCO_ {3}$↓$+ H_ {2}O $
(4)实验结论:CO2能溶于水,使塑料瓶内压强变小,外界大气压将塑料瓶压瘪了。
实验原理
$ CaCO_ {3} + 2HCl \stackrel {} {=} CaCl_ {2} + H_ {2}O + CO_ {2} $↑