- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 参观实验室
- 练习实验基本操作
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第四章 生命之源--水
- 4.1 我们的水资源
- 爱护水资源
- 水的净化和纯化
- 硬水及其软化
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第三章 维持生命之气--氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 催化剂
- 氧气的制取
- 分解反应
- 3.3 燃烧条件与灭火原理
- 燃烧与灭火
- 爆炸与防爆安全
- 3.4 物质组成的表示式
- 化学式和化合价
- 和化学式有关的计算
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 空气中有哪些成分
- 氮气和稀有气体有用吗
- 纯净物和混合物
- 保护空气
- 2.2 构成物质的微粒(1)--分子
- 2.3 构成物质的微粒(2)--原子和离子
- 原子
- 离子
- 2.4 辨别物质的元素组成
- 什么是元素
- 元素名称和符号
- 单质和化合物
- 元素周期表
- 第五章 燃料
- 5.1 洁净的燃料--氢气
- 5.2 组成燃料的主要元素--碳
- 碳有哪些单质
- 碳燃烧生成什么
- 5.3 二氧化碳的性质和制法
- 二氧化碳的性质
- 二氧化碳的制备
- 二氧化碳对人类生活的影响与碳循环
- 5.4 古生物的“遗产”--化石燃料
- 学生实验活动记录和报告
- 实验一 化学实验简单的基本操作
- 药品的取用
- 酒精灯的使用
- 玻璃仪器的洗涤
- 实验二 氧气实验室制取、性质与物质燃烧的条件
- 过氧化氢制取氧气
- 高锰酸钾制取氧气
- 实验三 二氧化碳实验室制取与性质
科粤版初三上学期化学
《4.2 水的组成》考点精粹
水的性质
水的性质
(1)水的物理性质
纯水是无色、无臭、清澈透明的液体。在1标准大气压下,水的熔点是0℃,沸点是100℃,水结成冰,密度变小(4℃时水的密度最大,为1g/cm3),浮在水面上。
(2)水的化学性质
①通电时水能分解生成氢气和氧气。
②水还能与某些物质反应。(如水能和二氧化碳反应生成碳酸,所以我们平时喝的汽水也叫碳酸饮料。)
水的电解实验
探究水的组成
实验目的 | 验证水的组成 |
实验仪器 | 电解器和直流电源等(如图所示) 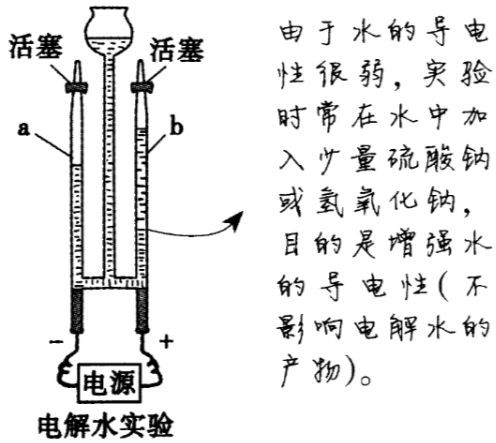 |
实验步骤 | 在电解器玻璃管里加满水,接通直流电源,观察并记录两个电极附近和玻璃管内发生的现象 |
实验现象 | 电极上均有气泡产生,通电一段时间后,两个玻璃管内收集了一些气体,与电源正极相连的玻璃管内的气体体积小,与电源负相连的玻璃管内的气体体积大,体积比约为1∶2(由于氧气在水中的溶解能力比氢气强,实验开始阶段,两支玻璃管内氧气和氢气的体积比小于1∶2,但最终氧气和氢气的体积比约为1∶2。) |
气体检验 | 切断电源,正极产生的气体用燃着的木条检验,观察到燃着的木条燃烧更旺,说明是氧气;负极产生的气体用燃着的木条检验,气体能燃烧,并产生淡蓝色的火焰,说明是氢气 |
文字表达式 | 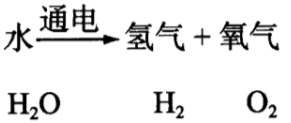 |
实验分析 | 氢气是由氢元素组成的,氧气是由氧元素组成的,根据化学反成前后元素种类不变的原理,可推断水不是由一种元素组成的,是由氢、氧两种元素组成的 |
实验结论 | (1)水在通电的条件下,发生了分解反应,生成了氢气和氧气 (2)水由氢元素和氧元素组成 |
说明:(1)用示意图的形式表示水电解的过程,如下图所示。
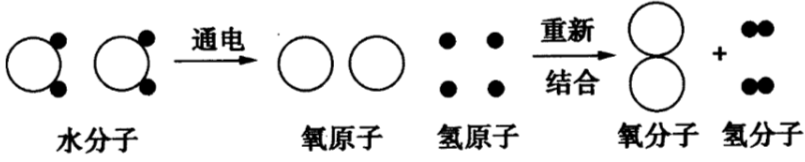
当水分子分解时,生成了氢原子和氧原子,2个氢原子结合成1个氢分子,很多氢分子聚集成氢气,2个氧原子结合成1个氧分子,很多氧分子聚集成氧气。
(2)水的电解图示证明:水是由氢、氧两种元素组成的;化学变化的实质:分子分裂成原子,原子重新组合生成新的分子;分子由原子构成;化学反应前后元素种类不变、原子种类不变和原子数量不变等。
(3)电解水实验也可以采用如下图所示简易装置。
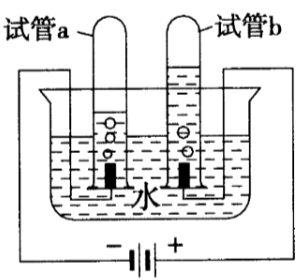
4.2 水的组成