- 身边的化学物质
- 空气和氧气
- 空气的成分
- 氧气的性质和用途
- 氧气的制取
- 水和氢气
- 自然界的水
- 氢气的性质及制取
- 碳和碳的化合物
- 碳单质
- 一氧化碳和二氧化碳
- 二氧化碳的实验室制法
- 金属与金属材料
- 金属材料
- 金属的化学性质
- 金属资源的利用与保护
- 生活中常见的化合物
- 常见的酸和碱
- 中和反应 pH
- 常见的盐
- 复分解反应
- 化学肥料
- 物质构成和变化
- 物质的分类
- 物质的微粒性
- 分子
- 原子
- 离子
- 元素
- 物质组成的表示
- 相对原子质量
- 相对分子质量
- 化学式
- 化合价
- 化学方程式
- 物质变化
- 物理变化与化学变化
- 化学反应类型
- 质量守恒定律
- 金属活动性顺序
- 溶液
- 化学基本实验与科学探究
- 常用化学仪器
- 化学实验基本操作
- 常见气体的实验室制取
- 物质鉴别
- 粗盐提纯
- 粗盐提纯
- 配制溶质质量分数一定的溶液
- 化学计算
- 有关化学式的计算
- 有关化学方程式的计算
- 有关溶液的计算
- 综合计算
- 化学与社会发展
- 人类重要的营养物质
- 化学元素与人类健康
- 有机合成材料
- 化学与能源
- 燃烧与灭火
- 化石燃料
- 能源的利用与开发
《元素》知识速查
元素
1.定义
元素是质子数(即核电荷数)相同的一类原子的总称。
质子数:决定元素的种类,即元素原子质子数不同,元素种类不同。
2.元素的种类
物质的种类非常多,已知的有几千万种,但是,组成这些物质的元素并不多,到目前为止,已经发现的元素只有一百多种。就像26个英文字母可以拼写出数十万个英文单词一样。有的物质组成中只有一种元素,如氧气(O2)和臭氧(O3),有的物质组成中有多种元素,如二氧化碳(CO2)高锰酸钾(KMnO4)、过氧化氢(H2O2)、碳酸钙(CaCO3)等。
说明:
(1)具有相同质子数的微粒不一定是同种元素,徽粒可能是分子、原子或离子。如水分子(H2O)和氖原子(Ne)都有10个质子,但不属于同种元素。
(2)这里所说的一类原子是指质子数相同、但中子数不一定相同的原子,也就是说同种元素的原子可以是质子数相同,但中子数不同的不同种原子,如$^{12}_{6}C$、$^{13}_{6}C$、$^{14}_{6}C$都是碳原子;质子数相同的原子与对应的单核离子,如氯原子和氯离子都属于氯元素。
(3)物质发生化学变化时,分子的种类发生变化,原子的种类不变,元素的种类也不会改变。
3.元素与原子的比较
元素 | 原子 | |
概念 | 具有相同质子数(即核电荷数)的一类原子的总称。一种元素可包含几种原子。如氢元素包含$^{1}_{1}H$、$^{2}_{1}H$、$^{3}_{1}H$ | 化学变化中的最小粒子 |
区别 | 宏观概念,只讲种类,不讲个数 | 微观概念,既讲种类,也讲个数 |
适用范围 | 描述物质宏观组成,如二氧化硫是由硫元素和氧元素组成的 | 用来描述由原子直接构成的物质和分子的构成。如铁是由铁原子构成的,1个水分子是由2个氢原子和1个氧原子构成的 |
联系 | 只要质子数(即核电荷数)相同的一类原子就属于同一种元素。原子元素的最小单位,元素则是原子的一个归类“集体”,即元素和原子是总体和个体的关系 | |
4.元素的存在
(1)空气中含量居前两位的元素是:氮、氧(按体积分数计算,氮气约78%,氧气约占21%)。
(2)生物细胞中含量居前四位的元素如下表所示。
元素 | 氧 | 碳 | 氢 | 氮 |
质量分数 /% | 65 | 18 | 10 | 3 |
(3)地壳中各种元素的含量分布如图所示。
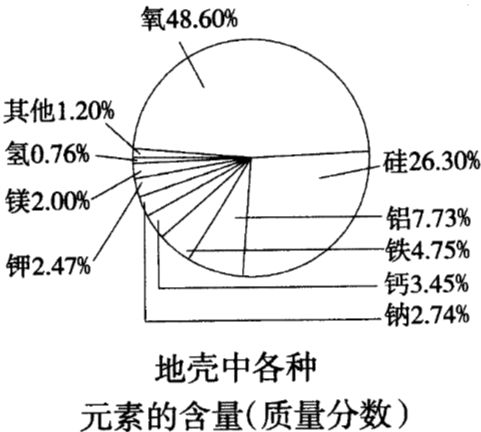
地壳中含量居于前四位的元素是:氧、硅、铝、铁。
(4)海水中含量居于前四位的元素是:氧、氢、氯、钠。
元素符号
1.元素符号的规定
国际上统一采用元素拉丁文名称的第一个字母(大写)来表示元素,如果几种元素拉丁文名称的第一个字母相同时,就附加一个小写字母来区别,如N表示氮元素,Na表示钠元素。
2.元素符号的写法
(1)由一个字母表示的元素符号要大写,如H、C、K、S等。
(2)由两个字母表示的元素符号,第一个字母大写,第二个字母小写,如Na、Mg、Cu等。书写这类元素符号时,特别注意要辨清第一个字母相同的一些类似的元素符号,如Cu、Ca、Cl等。
(3)常见元素符号规范写法如下:

3.元素符号的含义
(1)$意义\left\{\begin{array} {l} {\text {表示一种元素(宏观)}} \\ {\text {表示这种元素的一个原子(微观)}}\end{array}\right.$
$如H的意义\left\{\begin{array} {l} {\text {表示氢元素(宏观)}} \\ {\text {表示一个氢原子(微观)}}\end{array}\right.$
(2)对于由原子直接构成的物质,元素符号还表示一种物质。例如,Fe表示:铁元素;一个铁原子;铁这种物质。
(3)元素符号前面加化学计量数时,只能表示多个原子,不再表示这种元素,因为元素只讲种类不讲个数。如2N,只能表示两个氮原子,而不再表示氮元素,该符号只有微观含义。
4.元素的分类
元素分为三类:一是金属元素;二是非金属元素;三是稀有气体元素。
(1)金属元素:汉字名称偏旁为“钅”(金、汞除外),由金属元素组成的金属,通常状况下为固体,只有汞除外(通常状况下为液体),另外,金属由原子直接构成。
(2)非金属元素:通常状况下,非金属元素有三种状态,一是中文名称有“气”字头的,是气态非金属元素;二是中文名称有“氵”字旁的,是液态非金属元素;三是中文名称有“石”字旁的,是固态非金属元素。
(3)稀有气体元素:通常状况下,稀有气体为气体,它们的中文名称中都有“气”字头,它们是由原子直接构成的[如氦(He)]。
元素周期表
1.元素周期表
根据元素的原子结构和性质,将已知的一百多种元素按原子序数(数值上等于核电荷数)科学有序地排列起来所得的表,叫做元素周期表。
元素周期表中对金属元素、非金属元素(包括稀有气体元素)用不同的颜色做了区分,并标上了元素的相对原子质量。
2.元素周期表的结构
(1)横行(周期):元素周期表每一横行代表一个周期,共有7个横行,即7个周期。
(2)纵行(族):元素周期表共有18个纵行,每1个纵行叫做一个族,第8、9、10三个纵行共同组成一个族,所以有16个族。
(3)每一格:在元素周期表中,每一种元素均占据一格,每一格均包括元素的原子序数、元素符号、元素名称、相对原子质量等内容,还可推出质子数、电子数、元素的分类等信息,如图所示。
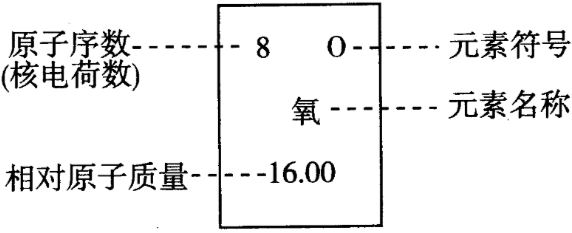
注意:
元素的原子核外有几个电子层,该元素就位于第几周期。如氧原子的结构示意图为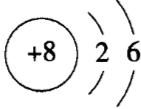 ,其原子核外有两个电子层,则氧元素位于第二周期。
,其原子核外有两个电子层,则氧元素位于第二周期。
原子序数=核电荷数=核内质子数=核外电子数
3.元素周期表的意义
(1)为寻找新元素提供了理论依据。
(2)由于元素周期表中位置越靠近的元素性质越相似,启发人们在元素周期表的一定区域内寻找新物质(如半导体材料、农药、催化剂等)。