- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究什么
- 物理变化和化学变化
- 物理性质和化学性质
- 空气中氧气含量的测定
- 混合物与纯净物
- 第3节 怎样学习和研究化学
- 常用的化学仪器及使用
- 化学实验的基本操作
- 物质性质的探究
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 空气的成分
- 氧气的性质
- 氧气的制法
- 催化剂和催化作用
- 第2节 奇妙的二氧化碳
- 自然界中的二氧化碳
- 二氧化碳的性质和用途
- 化合反应与分解反应
- 二氧化碳的制备与利用
- 第3节 自然界中的水
- 水的组成
- 水的净化
- 水资源的综合利用
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 微粒的性质
- 分子
- 原子
- 离子
- 第2节 组成物质的化学元素
- 元素与元素符号
- 物质的简单分类
- 元素与人体健康
- 第3节 物质的组成
- 化学式与化合价
- 化合物中元素之间的质量关系
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 燃烧与燃烧条件
- 爆炸与爆炸现象
- 防火与灭火
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与应用
- 化学反应的表示方法
- 根据化学方程式的计算
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 金属的性质
- 置换反应
- 合金
- 第2节 金属矿物 铁的冶炼
- 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
《第2节 化学反应中的质量关系》中考链接
化学反应的实质
分子、原子之间的区别和联系以及化学反应的实质是中考命题的热点之一;正确理解分子、原子的概念及本质区别,能够运用化学反应的微观实质去解释物理变化和化学变化,常见题型为选择题、填空题、简答题。
1单选题
双氧水分解的微观示意图如图所示,方框内应是( )
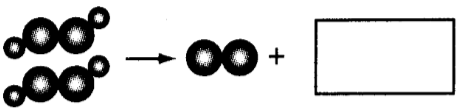
题目答案
您的答案
答案解析
问题要点
通过微观示意图的方式来考查化学反应的实质,化学变化都是分子分为原子,原子重新组合成新物质分子的过程。同时,还经常考查纯净物、混合物、分解反应、化合反应的微观实质。解此类习题,应首先弄清微观模拟示意图的含义,然后根据分子、原子的相关知识进行解答即可。
答案解析
双氧水分解生成水和氧气,由题图可以看出,![]() 是氧气分子,方框内物质应为水,
是氧气分子,方框内物质应为水,![]() 是氧原子,
是氧原子,![]() 是氢原子,水分子的结构示意图应为
是氢原子,水分子的结构示意图应为![]() ,根据化学反应前后原子种类、个数不变,可知方框内应生成2个水分子。
,根据化学反应前后原子种类、个数不变,可知方框内应生成2个水分子。
根据质量守恒定律确定物质的组成元素
考查质量守恒定律的应用。解答此类问题先根据反应前后元素种类不变,推断出物质中一定含有或可能含有的元素,再根据元素质量不变求出一定含有的元素的质量,与物质质量比较大小确定出可能含有的元素质量;根据元素质量与相对原子质量的比值可求出原子个数比从而确定出物质的化学式(或最简式),根据物质质量与相对分子质量的比值可求出分子个数比。
1单选题
某纯净物在9.6g氧气中恰好完全燃烧,生成8.8gCO2和5.4gH2O,下列说法正确的是( )
题目答案
您的答案
答案解析
由质量守恒定律可知,反应前后元素种类不变,该物质中一定含有碳元素和氧元素。8.8gCO2中含有氧元素的质量为$8.8 g \times ( \frac {16 \times 2} {44} \times 100 \% ) = 6.4 g$,5.4gH2O中含有氧元素的质量为$5.4 g \times ( \frac {16} {18} \times 100 \% ) = 4.8 g$,生成物8.8g二氧化碳和5.4g水中所含氧元素的质量之和为6.4g+4.8g=11.2g,11.2g>9.6g;该物质中含氧元素的质量为11.2g-9.6g=1.6g,则该物质中一定含有碳、氢、氧三种元素。



